LE RÉCEPTEUR AUX GLUCOCORTICOÏDES RÉGULE LE RYTHME CIRCADIEN DE LA SUSCEPTIBILITÉ AUX ARYTHMIES GRÂCE À LA MODULATION ÉPIGÉNÉTIQUE DE L’EXPRESSION DES CANAUX IONIQUES
Les études cliniques montrent que les arythmies ventriculaires liées à la mort subite cardiaque surviennent plus fréquemment le matin au réveil. Les mécanismes qui déterminent cette variation circadienne dans la susceptibilité aux arythmies ne sont pas connus.
Cette étude portée par l’équipe dirigée par Alicia D’Souza de l’Imperial College de Londres au Royaume Uni en collaboration avec le groupe « Cardioprotection, Physiopathologie du Rythme Cardiaque et Ischémie » animé par Matteo Mangoni a montré un rôle inattendu de l’hormone de stress cortisol dans ce phénomène. Les corticoïdes présentent un pic de concentration dans le plasma au début de la phase active (lumière éteinte chez la souris, levée du soleil chez les humains). Ceci induit une translocation du récepteur au glucocorticoïdes (GR) dans le noyau, conduisant à l’activation d’un programme spécifique de régulation génique qui conduit à une augmentation de l’expression des canaux ERG1 codant pour le courant potassique IKr et une réduction de l’expression des canaux sodiques voltage-dépendants cardiaques Nav1.5 codant pour le courant INa. De plus, une diminution de l’expression de la connexine43 (Cx43) qui régule la conductivité électrique entre les myocytes ventriculaires est observé au début de cette phase active. Une approche de modélisation in silico de l’excitabilité ventriculaire indique que ces changements favorisent la formation locale des circuits pro-arythmiques au début de la phase active. Il est intéressant de noter que cette régulation épigénétique de l’expression des canaux ioniques ventriculaire par les GR activés est indépendante de l’activité des gènes canoniques du rythme circadien tels que Per2 et Klf15. Il est toutefois probable que ces gènes canoniques changent l’état d’accessibilité de la chromatine peu avant le début de la phase active pour permettre l’action du GR. Ce travail fait partie du programme scientifique du réseau transatlantique Fondation Leducq FANTASY coordonné par Matteo Mangoni et propose, pour la première fois, un mécanisme épigénétique pour expliquer la variation circadienne de la susceptibilité aux arythmies et à la mort subite cardiaque.
Cette étude vient d’être acceptée pour publication dans le journal Circulation Research et a fait l’objet d’un Éditorial.
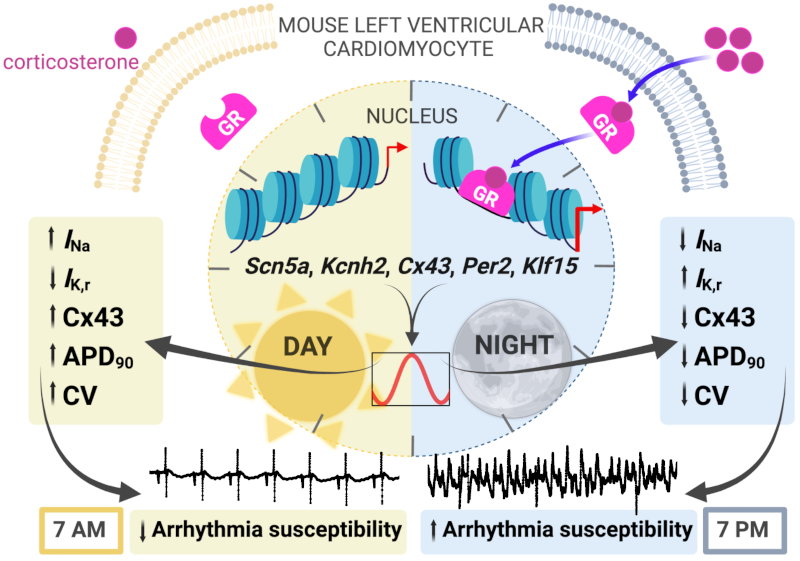
Dessin schématique montrant l’action des corticoïdes et leur récepteur inactif (panneau gauche), ou actif lié à la chromatine (panneau à droite) dans la régulation circadienne de l’expression des canaux ioniques et de la Cx43 la journée et la nuit (phase active de la souris). Le schéma montre le lien entre le changement dans l’expression génique et la susceptibilité aux arythmies ventriculaires. Les flèches indiquent la direction du changement dans l’expression d’un gène donné menant à un électrocardiogramme normal (gauche), ou arythmique (droite). Abréviations : Scn5a (canaux Nav1.5), Kcnh2 (canaux ERG1), APD90 (durée du potentiel d’action ventriculaire à 90% de la phase de repolarisation), CV (période réfractaire du ventricule).


