La plupart des athlètes d’endurance présentent une fréquence cardiaque au repos bien plus basse que celle de la population générale. La baisse de la fréquence cardiaque conséquente à l’entrainement d’endurance est attribuée à une augmentation du tonus du système nerveux parasympathique (tonus vagal). Ceci est le concept exposé dans les livres de texte de physiologie et de cardiologie, bien que le tonus vagal n’ait jamais fait l’objet de mesures directes chez les athlètes. La baisse de la fréquence cardiaque est aussi considérée comme une adaptation physiologique bénéfique à la suite de l’entrainement.
Les athlètes sont considérés comme la population bénéficiant d’une meilleure santé. Toutefois, des études cliniques récentes montrent que les athlètes présentent des dysfonctions du nœud atrioventriculaire (nœud AV) et une fréquence accrue du block de conduction auriculo-ventriculaire de premier et deuxième degré (bloc AV). Les bloc AV sont généralement bien tolérés par les jeunes athlètes, toutefois les études cliniques montrent une dérive pathologique au cours de leur vie. De ce fait, les athlètes présentent un risque accru de bradycardie (cœur trop lent) et nécessitent l’implantation d’un pacemaker électronique de façon plus fréquente que le reste de la population.
La vision généralement acceptée du rôle du tonus vagal dans le bloc auriculo-ventriculaire à la suite de l’entrainement, est remise en cause par une étude collaborative entre les Universités de Manchester et de Copenhague, en association avec l’équipe de Matteo Mangoni à l’IGF. Cette étude associe des résultats obtenus sur des chevaux de course, avec l’exploration d’un modèle murin d’entrainement d’endurance, pour démontrer que le bloc AV ne peut pas être attribué à une augmentation du tonus vagal, mais à un remodelage intrinsèque du nœud AV.
Ce remodelage implique une forte réduction de la transcription de gènes codant pour les canaux calciques de type L Cav1.2 et les canaux activés par l’hyperpolarisation HCN4, qui sont impliqués dans la génération du potentiel d’action et de la conduction électrique à l’intérieur du nœud AV. En particulier, ce remodelage est possible grâce à l’activation d’un profil d’expression des microRNA qui répriment l’expression de ces canaux ioniques. L’étude montre aussi que la suppression de l’activité de ces microRNA in vivo est capable de prévenir la dysfonction et les blocs AV.
En conclusion, cette étude démontre l’existence d’un nouveau mécanisme physiologique pour la régulation de la conduction de l’activité électrique cardiaque et elle indique aussi que les microRNA contrôlant l’expression des canaux ioniques pourraient être une nouvelle cible thérapeutique dans la prise en charge du bloc auriculo-ventriculaire.
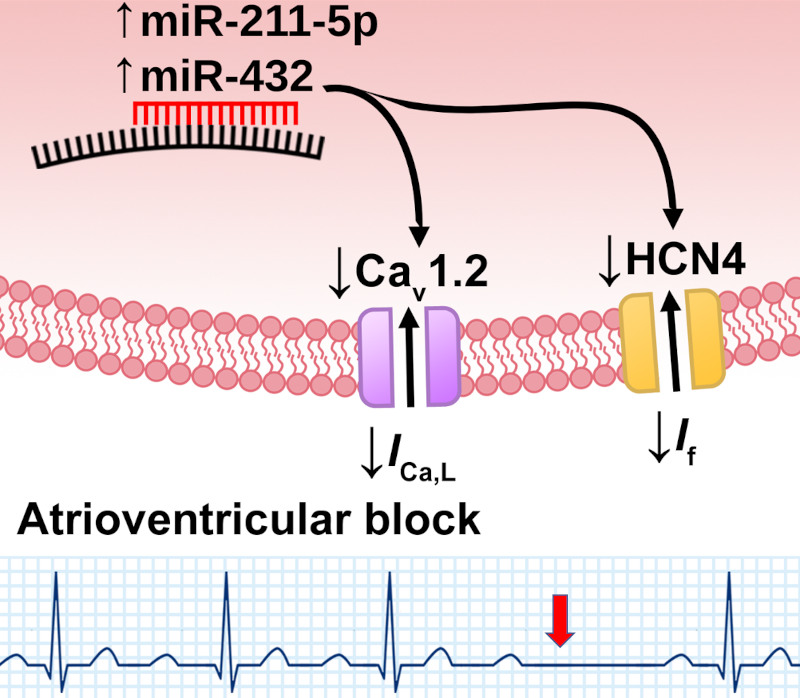
L’expression des microRNA (miR-211-5p and miR-432) qui contrôlent négativement l’expression de deux canaux ioniques importants pour la génération et la conduction du potentiel d’action atrioventriculaire est augmentée au cours de l’entrainement d’endurance. L’expression des canaux calciques de type L Cav1.2 et des canaux activés par l’hyperpolarisation HCN4 est diminué comme celle des courants ioniques que ces canaux génèrent (ICa,L et If).
Ceci est la cause du bloc AV (atrioventricular block), qui est visible sur l’électrocardiogramme idéalisé (panneau en bas) comme un battement ventriculaire manquant entre deux battement visibles (flèche).


