L’arginine vasopressine (AVP) est l’hormone antidiurétique, et elle régule une fonction vitale de notre organisme, l’équilibre hydrique. Elle agit au niveau du rein, plus précisément à la membrane plasmique des cellules principales du tubule collecteur, segment distal du néphron. C’est par son interaction avec le récepteur V2 (V2R), protéine membranaire de la famille des récepteurs couplés aux protéines G (RCPGs), que cette hormone peptidique active une voie de signalisation cellulaire qui conduit à une relocalisation des canaux à eau, les aquaporines, et donc à la réabsorption de l’eau de l’urine vers le sang. Le couplage du récepteur V2 à la protéine Gs constitue une étape clé de cette voie de signalisation.
Mais comment ça marche ?
C’est ce que vient de déterminer l’équipe de Bernard Mouillac et Sébastien Granier à l’Institut de Génomique Fonctionnelle (IGF), en collaboration avec l’équipe de Patrick Bron au Centre de de Biologie Structurale (CBS) par une approche de cryo-microscopie électronique. La stratégie des chercheurs combine également des données de RMN (résonance magnétique nucléaire) déterminées par Hélène Déméné (CBS) et des approches computationnelles de dynamique moléculaire développées par Nicolas Floquet à l’Institut des Biomolécules Max Mousseron (IBMM). C’est donc un travail 100% montpelliérain.
Cette approche intégrée de biologie structurale a permis de déterminer dans les moindres détails moléculaires comment l’AVP se fixe sur le récepteur pour activer la protéine Gs. La structure 3D du complexe ternaire composé de l’hormone naturelle, du récepteur V2 et de la protéine Gs n’avait encore jamais été déterminée expérimentalement.
Cette étude va plus loin que la simple description d’une structure d’un récepteur ou d’un complexe de signalisation. En effet, de nombreuses mutations du récepteur sont responsables de deux maladies génétiques rares présentant un tableau clinique inversé : 1/ le diabète insipide néphrogénique congénital (DINc) dû à des mutations « perte de fonction » associées à une incapacité des patients à concentrer leurs urines, 2/ le syndrome néphrogénique d’antidiurèse inappropriée (SNADI) lié à des mutations constitutivement actives caractérisé par une intoxication à l’eau et une hyponatrémie. Le V2R est également une cible primordiale pour traiter certaines formes de polykystose rénale, maladie beaucoup plus fréquente menant en général à une insuffisance rénale. Vis-à-vis de ces différentes pathologies, il y a donc un intérêt tout particulier à développer des outils thérapeutiques du V2R présentant une meilleure sélectivité, une meilleure efficacité, sans entraîner d’effets indésirables.
L’étude permet plus particulièrement de proposer d’un point de vue structural les conséquences de mutations ponctuelles du V2R. Par exemple, les chercheurs avancent des hypothèses pour expliquer pourquoi les mutants de l’acide aminé arginine 137 en leucine ou cystéine (R137L ou R137C) provoquent une activation constitutive du V2R et donc la maladie SNADI. Il est également tentant d’interpréter des observations cliniques, ou des données cellulaires et pharmacologiques in vitro sur la base des informations structurales du V2R. Par exemple, des hypothèses sont proposées pour expliquer les conséquences des mutations V88M (valine mutée en méthionine) ou M272R (méthionine mutée en arginine) responsables d’un DINc.
A l’avenir, la connaissance des détails atomiques des différentes conformations du récepteur V2 guidera le développement de nouvelles molécules thérapeutiques pour l’activer ou le bloquer. Cette perspective de recherche est cruciale vis-à-vis de maladies difficiles à gérer et accablantes pour les patients.
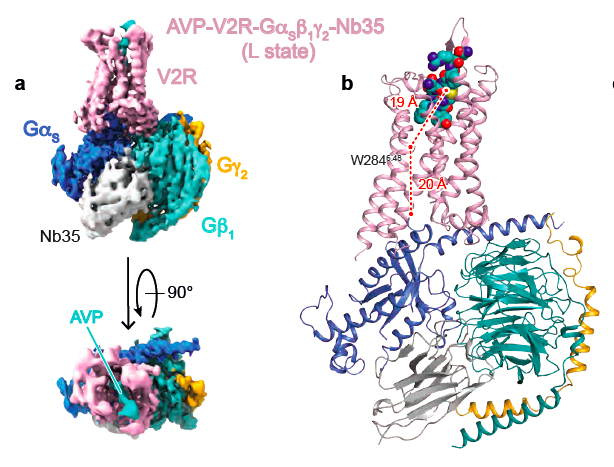
Carte de densité du complexe de signalisation AVP-V2R-Gs (A) et modèle 3D correspondant (B)


