La résistance antimicrobienne du staphylocoque doré (Staphylococcus aureus, SA) représente une grande menace pour la santé publique. De nouvelles cibles thérapeutiques sont donc nécessaires pour la conception d’antibiotiques innovants. Les leukotoxines secrétées par SA sont des cibles intéressantes car elles se lient aux récepteurs de l’hôte, notamment aux récepteurs des chimiokines présents à la surface des cellules immunitaires et érythrocytaires, une étape critique dans la pathogénicité de SA. En effet, cette liaison conduit à la destruction de ces cellules, ce qui permet au SA de diminuer la capacité de l’hôte à se débarrasser du pathogène et en même temps de fournir les éléments essentiels à la croissance bactérienne, notamment le fer présent dans les érythrocytes.
Pour mieux comprendre comment ces toxines agissent sur leur cible, l’équipe de Sébastien Granier à l’Institut de Génomique Fonctionnelle (CNRS/INSERM/Université de Montpellier), dans une étude co-dirigée par Chérine Bechara, a développé une approche intégrative de pharmacologie et de spectrométrie de masse structurale. Plus particulièrement, ce travail publié dans la revue Proc. Natl. Acad. Sci. décrit les mécanismes moléculaires de la liaison toxine/récepteur et son effet sur les conformations du récepteur, c’est à dire comment la toxine modifie la structure du récepteur pour pirater son activité.
Cette étude constitue donc une première étape vers le développement d’antibiotiques innovants qui bloqueraient le pouvoir pathogène de SA en inhibant la liaison aux récepteurs de l’hôte.
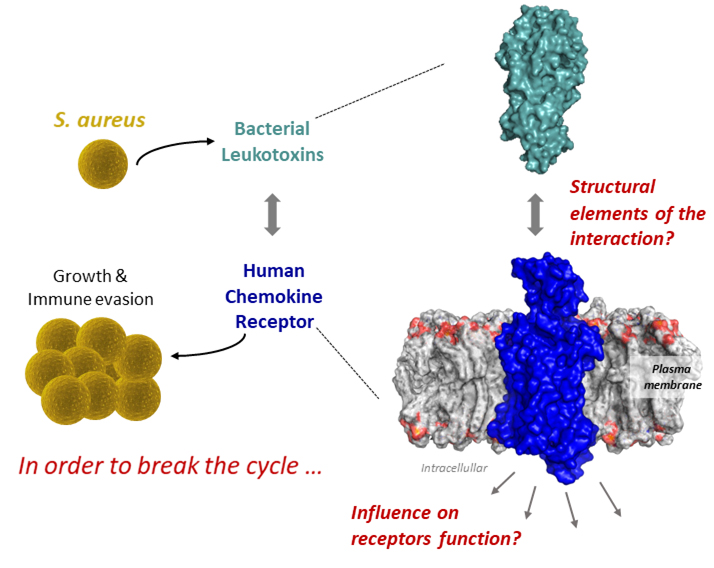
Structure et fonction des complexes leucotoxine/récepteur : une nouvelle fenêtre thérapeutique pour inhiber l’infection à SA


