UNE STRUCTURE CRYO-EM DU CANAL CALCIQUE CaV3.2 POUR MIEUX COMPRENDRE LES MODALITÉS DE LA SENSIBILITÉ PHARMACOLOGIQUE DES CANAUX CALCIQUES DE TYPE T
Les canaux ioniques sont la cible de nombreuses molécules d’intérêt thérapeutique. C’est le cas des canaux calciques de type T Cav3.2 : une cible prometteuse pour traiter entre autres certaines formes de douleur chronique et d’épilepsie, grâce au développement d’une nouvelle génération d’inhibiteurs plus sélectifs. Ces dernières années, notre compréhension du mécanisme d’action des modulateurs de canaux ioniques a été largement favorisée par la caractérisation structurale en cryo-EM de plusieurs de ces canaux ioniques. L’étude du groupe de Nieng Yan (Tsinguha University, Beijing) réalisée en collaboration avec Amaël Davakan et Philippe Lory (équipe « Canaux ioniques – Excitabilité neuronale et Canalopathies« ) présente la structure du canal Cav3.2 sous sa forme ‘apo’ ainsi que 4 structures obtenues en présence d’inhibiteurs sélectifs (TTA-P2, TTA-A2, ML-218 et ACT-709478). Ces données structurales identifient l’importance des interstices (‘fenestrations’) entre les 4 domaines transmembranaires par lesquels ces inhibiteurs rejoignent leur site de liaison se situant dans la cavité centrale du pore canalaire. Certaines drogues empruntent la ‘fenestration’ entre les domaines II et III, et c’est la ‘fenestration’ entre les domaines IV et I pour d’autres molécules. L’étude pointe également l’importance d’un résidu phénylalanine (Phe1007) dans la poche de liaison de ces inhibiteurs. Cette phénylalanine est parfaitement conservée entre les canaux de type T (Phe956 sur Cav3.1 et Phe854 sur Cav3.3). Dans son ensemble, cette étude apporte une vision structurale de la pharmacologie des canaux de type T en identifiant des déterminants moléculaires importants de la sélectivité et de l’affinité des bloqueurs. Ces travaux ouvrent la voie à la découverte de nouvelles molécules ciblant l’une ou l’autre des isoformes de Cav3, offrant ainsi de nouvelles perspectives thérapeutiques.
Cette étude vient d’être publiée dans le journal Cell Research.
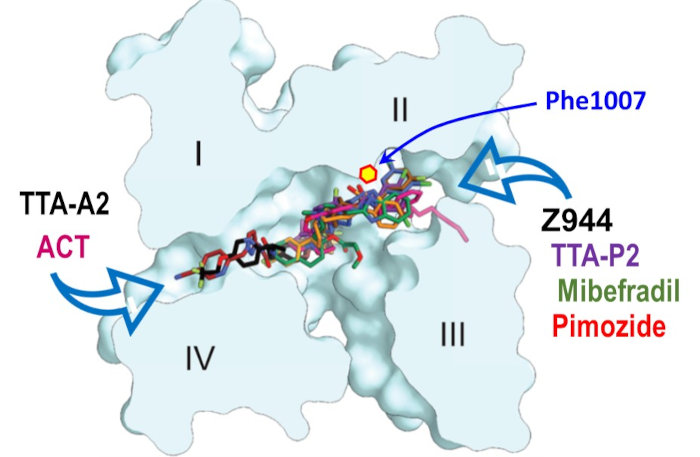
Cartographie structurale des sites de liaison des inhibiteurs des canaux Cav3 dans la cavité centrale du canal et leur positionnement respectif dans les fenestrations VI-I (TTA-A2 et ACT-709478) et II-III (Z944, TTA-P2, Mibefradil et Pimozide).


