INHIBITION SPÉCIFIQUE DES CANAUX CALCIQUES DE TYPE L CaV1.2 VERSUS CaV1.3 PAR LA TOXINE CALCISEPTINE ISSUE DU VENIN DE MAMBA NOIR
Les canaux calciques de type L sont impliqués dans de nombreuses fonctions physiologiques. Les cellules myocardiques expriment deux isoformes de canaux L à savoir Cav1.2 et Cav1.3. Cav1.2 est exprimé de façon ubiquitaire dans les tissus cardiaques ventriculaires et supraventriculaires incluant les nœuds sinoatrial (SAN) et atrioventriculaires (AVN). Cav1.2 est l’isoforme prédominante dans le ventricule adulte où il est responsable du couplage excitation-contraction et constitue la cible de la voie AMP- dépendante qui médie l’effet inotrope positif des catécholamines sur la contraction cardiaque. Cav1.3 est exprimé dans les oreillettes et en particulier fortement exprimé dans les cellules du SAN, du AVN et du tissu conducteur. Ainsi Cav1.3 joue un rôle majeur dans l’activité pacemaker du SAN et la conduction de l’influx dans le AVN. Malgré l’importance d’identifier les rôles physiologiques respectifs de Cav1.2 et Cav1.3 dans les tissus cardiaques mais aussi dans les cellules neuronales, il n’existe pas à l’heure actuelle d’outil pharmacologique sélectif disponible. Les venins animaux constituent un immense réservoir pour l’identification des toxines capables d’inhiber spécifiquement des isoformes de canaux ioniques et déterminer leur fonction dans divers tissus.
Un travail collaboratif impliquant trois équipes de l’IGF (équipe « Cardioprotection, physiopathologie du rythme cardiaque et ischémie » animée par Stéphanie Barrère et Matteo Mangoni, équipe « Dynamique cellulaire des canaux calciques et nociception » animée par Emmanuel Bourinet, équipe « Canaux Ioniques-Excitabilité neuronale et canalopathies » animée par Philippe Lory), l’Institut de Pharmacologie Moléculaire et Cellulaire à Valbonne (Université Côte d’Azur) ainsi que le Département de Physiologie de l’Université Nationale de Singapour, a permis de montrer que la calciseptine (Cas), un polypeptide issu du venin du mamba noir, bloque sélectivement les canaux Cav1.2, sans affecter les canaux Cav1.3. Cas diminue puissamment la contractilité cardiaque sans affecter la fréquence cardiaque d’un cœur de souris perfusé à Langendorff. Alors que Cas bloque totalement ICaL (Cav1.2) dans les myocytes ventriculaires, il inhibe partiellement le courant ICaL (ICav1.2+ICav1.3) dans les myocytes SAN de souris témoins mais bloque totalement ICaL dans les myocytes des souris Cav1.3-/-, où seul Cav1.2 est fonctionnel. La sélectivité du blocage par Cas de Cav1.2 par rapport à d’autres canaux calciques a été confirmée dans des HEK-293T exprimant des canaux recombinants Cav1.2, Cav1.3 (variants d’épissage Cav1.3 42a et Cav1.3 42), Cav3.1 (type T,) Cav2.2 (type N) et Cav2.1 (type P/Q).
En conclusion, cette étude montre que la calciseptine bloque sélectivement les canaux Cav1.2 dans le cœur et représente un outil important dans le panel des modulateurs des canaux calciques pour aider à disséquer le rôle de ces deux isoformes des canaux calciques L dans la physiopathologie cardiaque, mais aussi dans les cellules neuronales où chaque isoforme est décrite comme médiant des fonctions physiologiques spécifiques.
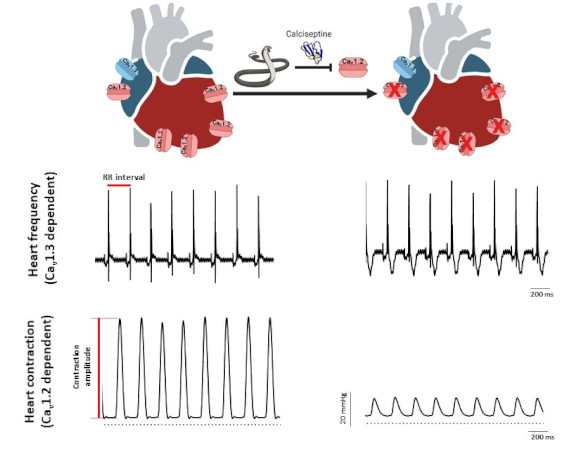
Fréquence cardiaque et contraction ventriculaire dans le cœur perfusé en présence de calciseptine. Tracés ECG (haut) et enregistrements de pression (bas) d’un cœur isolé perfusé, en condition contrôle (gauche) et en présence de calciseptine (droite).


