Équipe François RASSENDREN
Signalisation purinergique et inflammation du cerveau
Projet Réaction microgliale dans les pathologies neurologiques : diversité et potentiel thérapeutique
RESPONSABLE

Personnel IGF impliqué
Matthieu PRIEUR
Doctorant(e) UM
Coralie CLUA-PROVOST
Doctorant(e) UM
Valentin GARCIA
Doctorant(e) Inserm
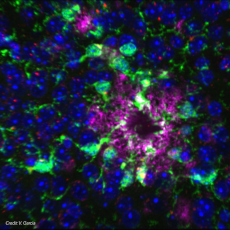
Les cellules microgliales sont reconnues comme des acteurs majeurs du fonctionnement cérébral. Fortement impliquées dans la surveillance du parenchyme nerveux, elles jouent un rôle clé dans le déclenchement des processus neuro-inflammatoires. Dotées d’un vaste éventail de récepteurs et de protéines transmembranaires, les microglies sont capables de détecter les changements dans l’environnement tissulaire et d’initier des signaux intracellulaires qui conduiront in fine à une réaction microgliale.
Notre groupe de recherche se concentre sur la compréhension des mécanismes d’initiation de la réaction microgliale, plus particulièrement dans contexte de la maladie d’Alzheimer.
Rôles fonctionnels de Clec7a dans les phases précoces de la Maladie d’Alzheimer
Diversité des cellules microgliales humaines dans la maladie d’Alzheimer
Diversité des cellules microgliales dans un modèle primate de la maladie d’Alzheimer
Rôles fonctionnels de Clec7a dans les phases précoces de la Maladie d’Alzheimer
Nos travaux antérieurs nous ont conduit à identifier Clec7a comme un marqueur précoce de la réaction microgliale dans la maladie d’Alzheimer. Néanmoins le rôle fonctionnel de ce récepteur reste majoritairement inconnu. Nos objectifs principaux sont de :
• Identifier le rôle fonctionnel de Clec7a dans le fonctionnement des cellules microgliales
• Déterminer s’il peut représenter une cible thérapeutique précoce dans le contexte de la maladie d’Alzheimer
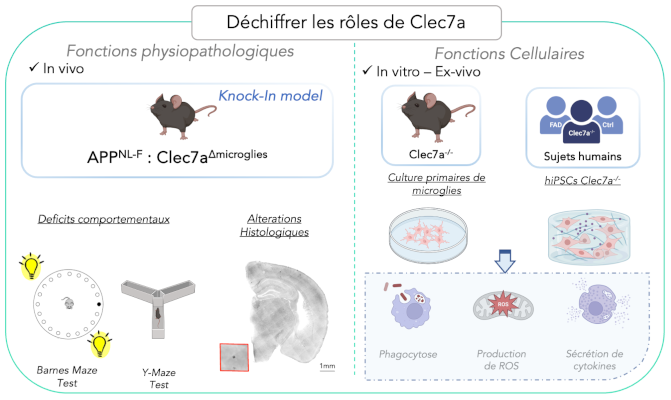
Déchiffrer les rôles fonctionnels de Clec7a dans les phases précoces de la maladie d’Alzheimer pour déterminer si ce récepteur peut représenter une cible thérapeutique.
Principales publications
• Hemonnot-Girard AL., et al.; Journal of Neuroinflammation. 2022;19(1):234.
• Hemonnot-Girard AL et al., Brain Behav Immun 2021 91: 404-417.
• Hemonnot AL et al., 2019 Frontiers in Aging Neuroscience.
Financements
• 2023-2025 Fondation Alzheimer – Coordinateur
• 2021-2023 France Alzheimer – Coordinateur
Collaborations
• Dr Carole Escartin (NeuroPsi, Paris-Saclay)
Alumni
• Anne-Laure Hemonnot (Thèse, 2017-2021)
Diversité des cellules microgliales humaines dans la maladie d’Alzheimer
Bien que les cellules microgliales murines et humaines soient très similaires, il existe des divergences moléculaires et fonctionnelles notoires, susceptibles d’expliquer, en partie, le fort taux d’échecs des essais cliniques notamment dans le contexte de la maladie d’Alzheimer.
L’objectif du projet est d’utiliser la technologie des hiPSCs pour générer des réseaux neuraux immunocompétents, contenant neurones, astrocytes, oligodendrocytes et microglies, et d’étudier l’hétérogénéité moléculaire et fonctionnelle des microglies humaines, dans les phases d’initiation de la pathologie.
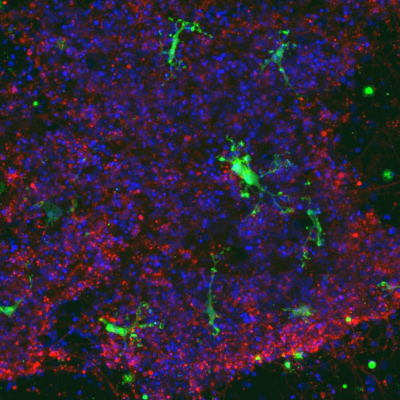
Les cellules microgliales humaines dérivées d’iPS (IBA1/ vert), en coculture avec des neurones dérivés d’iPS (βIII-tubuline/ rouge), présentent une morphologie ramifiée, typique de la microglie in vivo. Image acquise avec le microscope confocal Opera Phenix. Noyaux cellulaires colorés au DAPI (en bleu). Credit C. Clua-Provost/ Carole Crozet.
Principales publications
• Clua Provost C. et al. ; Stem Cell Res. 2023 73:103250.
Financements
• 2018-2021 Fondation Alzheimer – Coordinateur
• 2019 Prix de la Fondation Claude Pompidou – Partenaire
Collaborations
• Dr Carole Crozet (INM, Montpellier)
Diversité des cellules microgliales dans un modèle primate de la maladie d’Alzheimer
Pour surmonter les limitations inhérentes aux modèles murins, éloignés sur le plan génétique, et aux modèles cellulaires, par nature réductionnistes, une approche privilégiée consiste à utiliser des primates non-humains. Le Dr M. Dhenain et son équipe ont développé un modèle primate en inoculant, chez le microcèbe, des extraits de cerveaux de patients, reproduisant ainsi de nombreuses caractéristiques de la maladie. Au travers de cette collaboration nous cherchons à caractériser la diversité des états microgliaux dans ce modèle et à analyser leur évolution au cours de la progression de la pathologie.
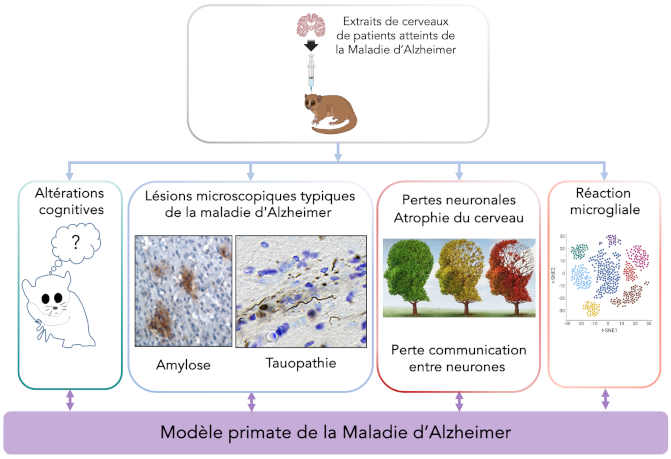
Le modèle “Microcèbe” de la maladie d’Alzheimer, un modèle innovant pour déchiffrer l’importance de la réaction microgliale dans cette pathologie.
Financements
• 2022-2026 ANR PrimAlz – Partenaire
Collaborations
• Dr Marc Dhenain (Laboratoire des maladies neurodégénératives, Kremlin-Bicêtre)


