Équipe Julie PERROY
Physiopathologie de la transmission synaptique
Projet Dynamique du réceptosome mGlu5 : implications dans la transmission et la plasticité synaptique
RESPONSABLE

Personnel IGF impliqué
Nathalie BOUQUIER
IE CNRS
Aragorn VELEZ
Doctorant CNRS
Pierre VINCENT
DR2 CNRS
Yan CHASTAGNIER
Doctorant UM
Julie PERROY
DR1 CNRS
Jeremie NAUDE
CRCN CNRS
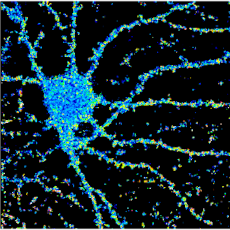
Nos travaux montrent que l’activité́ neuronale régule la dynamique des interactions moléculaires au sein du réceptosome glutamatergique. En retour, cette dynamique spécifie la signalisation des récepteurs, module la transmission synaptique et sous-tend les mécanismes de plasticité́ à long terme. On peut donc supposer que dans chaque épine, selon son contenu protéique, un signal donné va entrainer un remodelage particulier du réceptosome. Nous étudions la dynamique et l’influence de chacune de ces interactions sur le fonctionnement et la signalisation du récepteur, la transmission synaptique et les mécanismes de plasticité. Nous travaillons aussi sur des modèles cellulaires (dont des neurones dérivés des hiPSCs de patients) et murins de pathologies cérébrales dans lesquels la dynamique moléculaire est perturbée en cherchant à réparer l’interaction déficiente pour réguler finement et transitoirement la neurotransmission.
La plasticité synaptique dépend du renforcement de connexions synaptiques spécifiques entre les neurones. Mais pourquoi certains contacts synaptiques sont-ils renforcés et pas d’autres qui ont pourtant reçu le même signal ? L’hypothèse d’étiquetage synaptique et de capture propose que les synapses activées pendant la phase précoce de la plasticité sont étiquetées, ce qui leur permettrait de capturer les protéines nécessaires au maintien de la plasticité à long terme. L’ensemble de ces mécanismes permettrait l’engagement d’une synapse dans un réseau fonctionnel. Nos résultats préliminaires suggèrent que la dynamique des protéines du réceptosome mGlu5 pourrait permettre de sélectionner une épine et la maintenir dans un état potentialisé. Nous testons cette hypothèse en utilisant principalement des approches de BRET pour étudier la dynamique d’interaction des protéines d’intérêt en temps réel, à l’échelle de l’épine. Nous évaluons la plasticité par des approches de microscopie en super-résolution en mesurant le volume des épines dendritiques et l’insertion membranaire des récepteurs AMPA. Comme preuve de concept de l’importance de ces mécanismes moléculaires dans la cognition, nous cherchons également à réparer les interactions protéiques déficientes dans des modèles murins de Troubles du Spectre de l’Autisme.
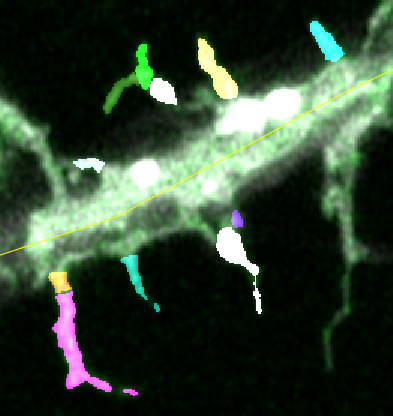
Identification des épines en imagerie super-résolution, dans le but de mesurer leurs variations de volume et l’insertion membranaire des récepteurs AMPA au cours de la plasticité.
Principales publications
• Moutin E., et al. (2021) Molecular Psychiatry. doi: 10.1038/s41380-021-01230-x
• Bouquier N., et al. (2020) BMC biology doi:10.1186/s12915-020-00790-8
• Moutin E., et al. (2016) Cerebral cortex. doi: 10.1093/cercor/bhw183
• Moutin E., et al. (2012) J Cell Biol, 2012. doi:10.1083/jcb.201110101
Financements
• Soutien à la recherche 2024 – programme d’excellence I-SITE
• ANR LEARN 2022
• ANR ISIBRAIN 2022
Collaborations
• Carlo Sala (Italie)
• Chiara Verpelli (Italie)


