Équipe Julie PERROY
Physiopathologie de la transmission synaptique

Par leur capacité à former et modifier leurs connexions synaptiques, nos neurones sont remodelés en permanence par nos expériences, ce qui modifie nos réseaux neuronaux fonctionnels et notre interaction avec l’environnement. Notre travail vise à comprendre comment l’apprentissage émerge de la plasticité, par une approche multi-échelle, de la dynamique des molécules synaptiques aux événements cellulaires et comportementaux qui déclenchent ou non de la plasticité. La compréhension de cette plasticité permet non seulement de découvrir de nouvelles thérapies dans les maladies neurologiques et troubles psychiatriques, mais apportent aussi des réponses à des questions fondamentales sur la cognition.
Nous recherchons les déterminants moléculaires et cellulaires qui régulent la formation, le fonctionnement et la plasticité des synapses, mais aussi la signalisation d’ensembles de neurones à l’origine de l’apprentissage des comportements. Cela nous permet d’aborder la question des troubles comportementaux, qu’ils résultent de facteurs génétiques ou environnementaux, sous l’angle des mécanismes moléculaire, cellulaires et de réseaux neuronaux.
La plasticité neuronale est un processus constamment actif : l’activité neuronale modifie des propriétés synaptiques, qui vont en retour changer l’activité des réseaux neuronaux. Nous nous focalisons donc sur la dynamique des protéines synaptiques impliquées dans l’adressage subcellulaire, l’assemblage membranaire et la signalisation des récepteurs du glutamate. Nos travaux antérieurs ont contribué à démontrer que les différentes fonctions d’un récepteur reposent sur sa capacité à s’engager dans des interactions protéine-protéine spécifiques avec des protéines d’échafaudage et effecteurs pour former une unité fonctionnelle appelée réceptosome. Ces interactions protéiques sont finement régulées, de manière très dynamique, par l’interaction avec l’environnement, et nécessitent donc d’être étudiées sous l’angle de la biologie des systèmes, en combinant prédictions issues de modèles théoriques et expérimentation de pointe. Par exemple, comprendre si un récepteur est activé en tant que molécule libre ou partie de différents complexes et quel est son rôle causal dans chacune de ces conditions sont des enjeux biologiques essentiels pour comprendre la logique fondamentale de la plasticité. Ces connaissances offrent aussi la possibilité de cibler exclusivement la voie de signalisation altérée dans une pathologie donnée.
Nos projets visent à caractériser la dynamique de molécules synaptiques, la logique du système de signalisation et de plasticité d’un neurone (et d’ensembles de neurones), et l’apprentissage comportemental qui en résulte. Nous travaillons au sein d’un cadre théorique formel (modélisation biophysique et cognitive) faisant le lien entre ces échelles. Cette approche permet d’une part de donner un cadre explicatif décrivant comment les propriétés à un niveau d’organisation (réseaux de neurones par exemple) émergent des niveaux inférieurs (interactions entre neurones, entre molécules) ; et d’autre part fournit des prédictions quantitatives (quelle forme de plasticité, quelle molécule impliquée) guidant nos expériences, qui répondent alors à des questions précises. Afin de caractériser ces différentes échelles d’organisation (molécules, neurone, réseau, comportement), nous développons des méthodes d’étude en temps réel de la dynamique d’interaction protéine-protéine et de la signalisation neuronale in vitro et in vivo, mais aussi des outils pour contraindre la dynamique moléculaire au niveau des synapses et comprendre leur importance physiologique et thérapeutique. Enfin, en tirant profit de modèles cellulaires et murins, nous promouvons une recherche translationnelle mécanistique, faisant l’aller-retour de la souris au patient. Pour proposer des cibles thérapeutiques, nous pouvons reproduire une mutation génétique identifiée chez un patient présentant des troubles du neurodéveloppement et/ou exposer les souris à un facteur environnemental, pour dépasser les corrélations entre facteurs et troubles, afin d’en comprendre la causalité.
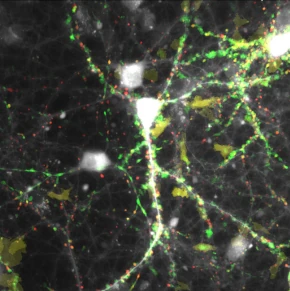
Projection des évènements calciques enregistrés pendant 2 minutes avec GCamP6s dans des neurones d’hippocampe, triés en fonction de leur taille et de leur propagation.

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10-
2011Habilitation à Diriger les Recherches (HDR) - Université de Montpellier - France
-
2001Doctorat - Biologie Cellulaire - Université de Montpellier - France
-
1998Master - Biologie Santé - Université de Montpellier - France
-
2020-Directrice de Recherche CNRS (DR1) - Institut de Génomique Fonctionnelle (IGF) - Montpellier - France
-
2015-Responsable de l’équipe "Physiopathologie de la transmission synaptique" - Institut de Génomique Fonctionnelle (IGF) - Montpellier - France
-
2012-2020Directrice de Recherche CNRS (DR2) - Institut de Génomique Fonctionnelle (IGF) - Montpellier - France
-
2004-2012Chargée de Recherche CNRS - Institut de Génomique Fonctionnelle (IGF) - Montpellier - France
-
2002-2004Postdoctorante (Dir. M. Bouvier) - Université de Montréal - Canada
-
1998-2001Doctorante - Centre CNRS INSERM de Pharmacologie-Endocrinologie (CCIPE) - Montpellier - France
- Distinctions
-
2015-2021ERC consolidator
-
2002-2004Bourse EMBO
-
2002Prix de thèse de la société des neurosciences
- Responsabilités
-
2022-2027Membre du collège des experts d’Aviesan, ITMO Neurosciences
-
2021-2024Membre du conseil administratif de la société française des neurosciences
-
2019-2025Coordinatrice du Conseil Scientifique du centre d’excellence sur l’autisme et les maladies neurodéveloppementales
-
2017-2022Membre du Conseil Scientifique de l’INSERM
-
2015-2018Membre du comité d’évaluation CE16 de l’ANR (Neurosciences mol et cell)
- L'originalité de notre travail réside dans le développement d'outils innovants pour élucider la dynamique et le rôle des interactions protéine-protéine autour des récepteurs. Nous avons en effet contribué à démontrer que les différentes fonctions d'un récepteur reposent sur sa capacité à interagir spécifiquement avec des protéines d'échafaudage et des effecteurs pour former une unité fonctionnelle appelée réceptosome. Ces interactions protéine-protéine sont finement régulées, de manière très dynamique, par les stimuli environnants.
- Mon équipe s'intéresse depuis de nombreuses années au rôle des réceptosomes, notamment des récepteurs métabotropiques au glutamate (mGlu). Pour élucider la dynamique spatio-temporelle des complexes protéiques associés aux récepteurs mGlu dans les neurones, nous avons développé et utilisé des approches biophysiques de pointe. Nous avons ensuite contraint la dynamique des interactions protéine-protéine au sein du réceptosome glutamatergique (en utilisant des outils moléculaires/pharmacologiques ou des souris transgéniques) pour comprendre leurs fonctions dans des conditions physiologiques et pathologiques.

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10-
2011Doctorat - Neurosciences - Université de Montpellier - France
-
2008Master - Biologie Santé - Université de Montpellier - France
-
2022-Chargée de Recherche au CNRS (CRCN) - Institut de Génomique Fonctionnelle - Montpellier - France
-
2016-2021Postdoctorante - Institut de Génomique Fonctionnelle - Montpellier - France
-
2012-2015Postdoctorante - Université de Genève - Suisse
-
2008-2012Doctorante - Institut de Génomique Fonctionnelle - Montpellier - France
-
2014Prix lors de la journée "Les grandes avancées du Pôle Rabelais" - Montpellier
- Je suis une neuroscientifique spécialisée dans l’étude des mécanismes moléculaires qui permettent de moduler la plasticité synaptique. Je m’intéresse aux séquences d’évènements qui ont lieu dans les épines dendritiques des synapses glutamatergiques pendant la plasticité, depuis les changements d’interaction protéiques, de localisation des protéines jusqu’aux remaniements morphologiques des épines.
- L’objectif à long terme est de mieux comprendre le rôle de la dynamique moléculaire associée au récepteur mGlu5 dans la localisation de la mémoire, en portant également un intérêt particulier aux modèles murins de Troubles du Spectre Autistique. En effet, il existe de nombreux modèles de TSA dans lesquels certaines protéines associées au récepteur mGlu5 sont mutées. Ces modèles sont de véritables outils permettant d’étudier d’une part l’importance de ces protéines dans la plasticité et d’autre part de trouver des stratégies pour moduler leur dynamique moléculaire dans le but de restaurer les défauts de plasticité et certains troubles cognitifs associés à ces pathologies.
- Les techniques que j’utilise principalement sont :
- Cultures primaires et tranches d’hippocampe
- BRET en imagerie
- Biochimie
- Biologie moléculaire
- Imagerie calcique
- Imagerie super-résolution
- Electrophysiologie

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10-
2022Habilitation à Diriger des Recherches (HDR) - Sorbonne Université - Paris - France
-
2010Doctorat en Neurosciences Computationnelles - Sorbonne Université (ex. Pierre et Marie Curie) - Paris - France
-
2007Master en Biologie Intégrative et Physiologie (Neuroscience) - Sorbonne Université (ex. Pierre et Marie Curie) - Paris - France
-
2021-Chargé de Recherche CNRS - Institut de Génomique Fonctionnelle - Montpellier - France
-
2016-2021Chargé de Recherche CNRS - Neuroscience Paris Seine - Paris - France
-
2012-2016Postdoctorant - Neuroscience Paris Seine - Paris - France
-
2010-2012ATER - Institut des Systèmes Intelligents et de Robotique - Paris - France
-
2007-2010Doctorant - Institut des Systèmes Intelligents et de Robotique - Paris - France
-
2023-Membre élu de la Société Française des Neurosciences
-
2022-Membre élu du Comité National du CNRS (section 26)
-
2014-2016Membre élu du Conseil du laboratoire - Neuroscience Paris Seine
-
2008-2009Membre étudiant élu du conseil de l’Ecole Doctorale - Sorbonne Université
-
2007-2009Membre étudiant élu de l’UFR de Biologie - Sorbonne Université
- Je suis neuroscientifique avec une double expertise en électrophysiologie/comportement in vivo et en modélisation informatique.
- Mes intérêts de recherche comprennent :
- - la neuromodulation, la plasticité, ce qui relie les échelles de temps électriques et comportementales
- - les modèles multiniveaux (voies intracellulaires, biophysique neuronale, réseaux neuronaux, cognitifs/comportementaux)
- - le cortex préfrontal et ses nombreux partenaires
- Techniques de laboratoire in vivo
- - Chirurgie stéréotaxique pour l'implantation d'électrodes, l'injection de virus, etc.
- - Enregistrements électrophysiologiques (in vivo sur des animaux en comportement, avec des tétrodes ou des sondes en silicium)
- - Essais comportementaux affinés (libre, opérant, décision, mémoire, etc.)
- Analyse des données
- - Sorting et clustering des potentiels d’action (PA)
- - Analyses dynamiques pour les séries temporelles discrètes (PA) et continues (EEG, calcium)
- - Analyse EEG/LFP (Fourier, cohérence, ondelettes, couplage cross-fréquences, etc.)
- - Analyses comportementales (choix, mouvements, etc.)
- Modélisation informatique
- - Construction de modèles
- - Ajustement des modèles aux données expérimentales (par exemple, comparaison de modèles)
- - Simulations (Matlab, Pyhton)
- - Analyse (champ moyen, analyse de bifurcation)Je suis neuroscientifique avec une double expertise en électrophysiologie/comportement in vivo et en modélisation informatique.
- Mes intérêts de recherche comprennent :
- la neuromodulation, la plasticité, ce qui relie les échelles de temps électriques et comportementales
- les modèles multiniveaux (voies intracellulaires, biophysique neuronale, réseaux neuronaux, cognitifs/comportementaux)
- le cortex préfrontal et ses nombreux partenaires
- Techniques de laboratoire
- Formation Concepteur Niveau 1 et Chirurgie
- Analyse de données
- Sorting et clustering des potentiels d’action (PA)
- Analyses dynamiques pour les séries temporelles discrètes (PA) et continues (EEG, calcium)
- Analyse EEG/LFP (Fourier, cohérence, ondelettes, couplage cross-fréquences, etc.)
- Analyses comportementales (choix, mouvements, etc.)
- Modélisation informatique
- Construction de modèles
- Ajustement des modèles aux données expérimentales (par exemple, comparaison de modèles)
- Simulations (Matlab, Pyhton)
- Analyse (champ moyen, analyse de bifurcation)

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10-
2011Habilitation à Diriger des Recherches (HDR) - Université Pierre-et-Marie-Curie (UPMC) - Paris - France
-
1994Docteur en Pharmacologie Moléculaire et Cellulaire - Université Paris 6 - France
-
1991Magistère à l'École Normale Supérieure de Lyon - France
-
2012-Directeur de Recherches au CNRS (DR2) - Institut de Génomique Fonctionnelle (IGF) - Montpellier - France
-
1996-2012Chercheur au CNRS
-
1994-1996Postdoctorant (Dir R.Y. Tsien) - Univ. of California San Diego - USA
-
1993Scientifique du contingent (Dir. J.P. Changeux) - Institut Pasteur - Paris - France
-
1991-1994Doctorant (Dir. A. Marty) - Laboratoire de Neurobiologie - École Normale Supérieure - Paris - France
-
2005-2022Responsable ou co-responsable d’équipe à Sorbonne Université
- Je m’intéresse aux aspects dynamiques de la signalisation intracellulaire et aux mécanismes d’intégration des signaux neuromodulateurs dans les neurones du système nerveux central. En particulier, j’ai analysé les spécificités de l’intégration de signaux dopaminergiques via la voie de signalisation AMPc/PKA dans les neurones du striatum, avec un intérêt particulier pour le rôle joué par les phosphodiestérases dans cette intégration.
- Imagerie de biosenseurs
- Biosenseurs codés génétiquement de la série AKAR, Epac…
- Imagerie de biosenseurs dans des préparations de tranches de cerveau
- Analyse de données
- Développement d’un ensemble logiciel pour l’analyse des données d’imagerie de biosenseur.
- Programmation dans l’environnement Igor Pro
- Gestion de données
- Base de données Filemaker Pro pour la gestion et le suivi des données numériques du laboratoire
- Electrophysiologie
- Patch-clamp sur cellules primaires, tranches de cerveau…
- Analyse de la transmission synaptique

 IGF Sud 227
IGF Sud 227
-
2003Ingénieur Génie Biochimique et Biomoléculaire, Génétique Microbienne - INSA (Institut National des Sciences Appliquées) - Toulouse - France
-
2011-Ingénieur CNRS - Institut de Génomique Fonctionnelle (IGF) - Montpellier - France
-
2004-2011Ingénieur Valorisation CNRS (CDD) - Centre de Recherche en Biologie Cellulaire de Montpellier (CRBM) - France
-
2015-2020Membre du Conseil de Laboratoire (nommé) - Institut de Génomique Fonctionnelle - Montpellier
-
2014-Responsable L2/L1 - Institut de Génomique Fonctionnelle - Montpellier
- En tant qu’ingénieur, je suis chargée d’élaborer et de mettre en œuvre les approches moléculaires des projets de l’équipe en combinant des techniques de biochimie, de biologie moléculaire et cellulaire pour déchiffrer et moduler les voies de signalisation de la plasticité neuronale et leurs dysfonctionnements associés aux troubles du spectre autistique.
- En particulier, je conçois et développe un ensemble d’outils moléculaires (biosenseurs, actuateurs, peptides TAT) pour visualiser et manipuler la dynamique d’interactions de protéines synaptiques.
- Principales techniques
- Biologie moléculaire : clonages (CRISPR, Gibson, Gateway), mutagenèse dirigée, séquençage, PCR, purification ADN / ARN, génotypage
- Biochimie des protéines : Production de protéines recombinantes, Western-blot, immunoprécipitation, interactions, dosage…
- Culture cellulaire : Cultures primaires de neurones / lignées cellulaires / iPSCs, transfection, transduction
- Production de lentivirus et AAV
- Microscopie : Live cell imaging, BRET, Immunomarquages (IF, IHC)
- Utilisation de logiciels scientifiques (traitement des données, acquisition et analyse d’images : Metamorph, AxioVision, ImageJ, statistiques : GraphPad Prism)
- Formations
- Référent L2/L3
- Concepteur Niveau 1
- Management de Projets

 IGF Nord 223
IGF Nord 223 04 34 35 92 10
04 34 35 92 10

 IGF Nord 223
IGF Nord 223 04 34 35 92 77
04 34 35 92 77

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10-
2024Master Biologie-Santé - Parcours Neurosciences - Université de Montpellier - France
-
2022Licence de Physiologie Animale et Neurosciences - Université de Montpellier - France
- Doctorante - Institut de Génomique Fonctionnelle - Montpellier - France
-
2024Stage de Master 2 (Dir. S.Trouche - eq S.Trouche) - Institut de Génomique Fonctionnelle - Montpellier - France
-
2023Stage de Master 1 (Dir. J.Naude - eq J.Perroy) - Institut de Génomique Fonctionnelle - Montpellier - France
- Mission Complémentaire d'Enseignement
- Comportement animal (Conditionnement opérant, conditionnement pavlovien, optogénétique...)
- Immunohistochimie
- Technique et analyse d'imagerie (Apotome, QuPath...)
- Analyse par Modèle (Matlab, Python...),
- Analyses de Données (GraphPad, Pack Office...)

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10

 IGF Sud 227
IGF Sud 227 04 34 35 92 10
04 34 35 92 10

 IGF Sud 223
IGF Sud 223 04 34 35 92 12
04 34 35 92 12
ALUMNI
• Sophie Sakkaki – Préparation de l’Agrégation en SVT
• Noémie Cresto – Chercheuse en Neurosciences (Post-doc, IGF Montpellier, France)
• Benoît Girard – Chercheur en Neurosciences (Université de Genève, Suisse)
• Marin Boutonnet – Chercheur en Neurosciences (Post-doc, Humboldt Université de Berlin, Allemagne)
• Roza Szlendak – Chercheuse en Neurosciences (IMC, warsaw, Pologne)
• Federica Giona – Spécialiste recherche et développement (recherche d’emploi, Milan Italie)
• Federica Bertaso – Chercheuse en Neurosciences (CRCN INSERM – IGF Montpellier, France)
• Jeanne Ster – Chercheuse en Neurosciences (CRCN CNRS – IGF Montpellier, France)
• Elise Goyet – Educatrice spécialisée (Lyon, France)
• Fabrice Raynaud – Enseignant chercheur (Université de Montpellier, France)
• Laura Ceolin – Attachée de recherche Clinique (Mediaxe Formation, Paris, France)
• Selma Dadak – Chercheuse en Neurosciences (Sensorion, Montpellier, France)
• Valériane Tassin – Webmaster (France)
• Adeline Burguière – Enseignante cours particuliers (Matha2, Montpellier, France)
• Jonathan Roger – Responsable des opérations cliniques (Paraxel, Montreal, Quebec, Canada)
- Boutonnet, M., Carpena, C., Bouquier, N., Chastagnier, Y., et al. (2024). Voltage tunes mGlu5 receptor function, impacting synaptic transmission. J. of Pharmacol. – in press
- Sakkaki, S., Cresto, N., Chancel, R., Jaulmes, M., Zub, E., Blaquière, M., et al. (2023). Dual-Hit: Glyphosate exposure at NOAEL level negatively impacts birth and glia-behavioural measures in heterozygous shank3 mutants. Environ Int doi: 10.1016/j.envint.2023.108201
- Areias, J., Sola, C., Chastagnier, Y., Pico, J., Bouquier, N., Dadure, C., et al. (2023). Whole-brain characterization of apoptosis after sevoflurane anesthesia reveals neuronal cell death patterns in the mouse neonatal neocortex. Sci Rep doi: 10.1038/s41598-023-41750-w
- Bousseyrol, E., Didienne, S., Takillah, S., Prevost-Solié, C., Come, M., Ahmed Yahia, T., et al. (2023). Dopaminergic and prefrontal dynamics co-determine mouse decisions in a spatial gambling task. Cell Rep doi: 10.1016/j.celrep.2023.112523
- Moutin, E., Sakkaki, S., Compan, V., Bouquier, N., Giona, F., Areias, J., et al. (2021). Restoring glutamate receptosome dynamics at synapses rescues autism-like deficits in Shank3-deficient mice. Mol Psychiatry. doi: 10.1038/s41380-021-01230-x
- Sarazin, M. X. B., Victor, J., Medernach, D., Naudé, J., and Delord, B. (2021). Online Learning and Memory of Neural Trajectory Replays for Prefrontal Persistent and Dynamic Representations in the Irregular Asynchronous State. Front Neural Circuits doi: 10.3389/fncir.2021.648538
- Mota, É., Bompierre, S., Betolngar, D., Castro, L. R. V., & Vincent, P. (2021). Pivotal role of phosphodiesterase 10A in the integration of dopamine signals in mice striatal D1 and D2 medium-sized spiny neurones. British Journal of Pharmacology, 178(24). doi: 10.1111/bph.15664
- Bouquier, N., Moutin, E., Tintignac, L., Reverbel, A., Jublanc, E., Sinnreich, M., et al. (2020). AIMTOR, a BRET biosensor for live imaging, reveals subcellular mTOR signaling and dysfunctions. BMC Biol. Jul 3;18(1.
- Sebastianutto, I., Goyet, E., Andreoli, L., Font-Ingles, J., Moreno-Delgado, D., Bouquier, N., et al. (2020). D1-mGlu5 heteromers mediate noncanonical dopamine signaling in Parkinson’s disease. Journal of Clinical Investigation 130, 1168–1184. doi: 10.1172/JCI126361
- Nair, A. G., Castro, L. R. V., El Khoury, M., Gorgievski, V., Giros, B., et al. (2019). The high efficacy of muscarinic M4 receptor in D1 medium spiny neurons reverses striatal hyperdopaminergia. Neuropharmacology (2019) 1. doi: 10.1016/j.neuropharm.2018.11.029
Dynamique du réceptosome mGlu5 : implications dans la transmission et la plasticité synaptique
Responsable
Enora MOUTIN
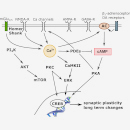

Les modèles cellulaires et murins permettent de mieux comprendre les mécanismes moléculaires et cellulaires à l’origine de troubles comportementaux et de tester des pistes thérapeutiques. Plusieurs situations cliniques sont ainsi à l’étude au laboratoire.
- Troubles du spectre de l’autisme (TSA) : Des troubles du neurodéveloppement et /ou de cognition sont générés par une mutation de gènes codant pour des protéines synaptiques, comme les récepteurs du glutamate (GRIN2B), des protéines d’échafaudage qui contrôlent leur fonction (SHANK3) ou encore de facteurs régulant l’expression des gènes au cours de la plasticité (FMR1). D’autre part, nous étudions aussi l’impact de facteurs environnementaux portant atteinte au fonctionnement cérébral, facteurs aussi variés que l’exposition à des pesticides (Glyphosate), à un virus (SARS-CoV-2), ou encore à un stress.
- Hémorragie Sous-Arachnoïdienne : L’hémorragie sous-arachnoïdienne par rupture d’anévrisme est fréquemment suivie d’ischémie cérébrale retardée, grevant fortement le pronostic des patients. La physiopathologie de cette complication est actuellement mal comprise. Nous cherchons à explorer, dans un modèle expérimental, les défauts microvasculaires et la réponse microgliale à l’hémorragie sous-arachnoïdienne en utilisant la microscopie in vivo, l’IRM, la transparisation de tissus et la transcriptomique. Dans une approche translationnelle, nous étudions également les marqueurs de ces phénomènes chez les patients en utilisant l’IRM et l’imagerie en TEP dynamique.
- Agents anesthésiques généraux : L’anesthésie générale provoque des changements radicaux dans l’activité neuronale de l’ensemble du cerveau. Ces changements peuvent s’accompagner de modifications à moyen/long terme des fonctions cellulaires. Nous étudions des voies de signalisation d’intérêt en utilisant des méthodes de transparisation de tissus et d’immunohistochimie. Des structures identifiées comme pertinentes sont ensuite caractérisées à l’aide d’un panel d’approches comprenant notamment des enregistrements électrophysiologiques extracellulaires in vivo.
Financements en cours
• ANR (2023-2027) LEARN “Light on intracellular signaling Events shAping functional netwoRks in spatial mapping”
• ANR (2023-2027) IsiBRAIN “Impact of SARS-CoV-2 Infection on the central nervous system”
• ANR (2024-2028) TimeTag “Timed decisions: underlying neural mechanisms and TAGging of neuronal ensembles in the prefrontal cortex”
• ANR (2020-2024) Glyflore “Impact of a chronic dietary exposure to low-doses of glyphosate on the gut microbiota and microbiota-associated physiological functions”
• CCA-Inserm-Bettencourt (2022-2026) “Role of microcirculatory damage in delayed cerebral ischaemia complicating aneurysmal subarachnoid haemorrhage”
• FRC (2024-2026) “Multiscale scientific method to fully characterize the functional consequences of GRIN variants, from biological mechanisms to brain diseases”
• FRM (2023-2026) “Role of mGlu5 receptosome dynamics in plasticity, metaplasticity and flexibility – Alleviation of autism spectrum disorders by molecular tinkering”
• MUSE (2020-2024) “Environmental pesticides and genetic predisposition: a path toward autism spectrum disorders “
• MUSE (2024) STRESSA “Combined effects of environmental stress and genetic predisposition to Autism Spectrum Disorders”
Collaborations en cours
 • Cathie Ventalon (IBENS, Paris France)
• Cathie Ventalon (IBENS, Paris France)
• Raphael Gaudin (IRIM, Montpellier France)
• Stéphanie Trouche (IGF, Montpellier France)
• Bruno Delord (ISIR, Paris France)
• Nicola Marchi et Etienne Audinat (IGF, Montpellier France)
• Sandrine Ellero-Simatos et Laurence Payrastre (INRAe, Toulouse France)
• Dorota Hoffman (IMC, Warsaw, Poland)
• Chiara Verpeli et Carlo Sala (CNS, Milano Italie)
• Amaria Baghdadli (CRA, CHU Montpellier France)
• Hélène Hirbec (IGF, Montpellier France)
• Noura Faraj (LIRMM, Montpellier France)
• Christophe Goze-Bac (L2C, Montpellier France)
• Bertrand Wattrisse (LMGC, Montpellier France)
• Emmanuelle Le Bars (I2FH, Montpellier France)
• Denis Mariano-Goulart (CHU, Montpellier France)
- des biosenseurs de voies de signalisation impliquées dans la plasticité neuronale (Fluorescence, BRET, FRET), avec pour ambition de combiner les lectures de plusieurs voies de signalisation (multiplexage), de manière simultanée.
- des actuateurs pour forcer, empêcher ou réparer la dynamique moléculaire synaptique et comprendre sa pertinence physiologique et thérapeutique.
- des routines d’automatisation de l’acquisition et de l’analyse d’images, pour résoudre la complexité d’un simple signal, et les intrications de multiples stimuli.
- de nouvelles technologies, comme l’imagerie BRET en cellules vivantes pour une localisation subcellulaire de la dynamique des protéines en temps réel, mais aussi le BRET in vivo pour enregistrer des signalisations d’ensemble de neurones chez l’animal au cours de comportements.