Équipe Emmanuel PÉRISSE
Circuits neuronaux et codage de la valeur

L’objectif principal de mon équipe est de décrypter la manière dont la valeur est attribuée aux stimuli sensoriels au cours de l’apprentissage pour être ensuite utilisée pour prendre des décisions économiques appropriées basées sur la valeur. Pour comprendre ces processus cérébraux conservés au fil de l’évolution, l’équipe utilise la mouche du fruit Drosophila melanogaster comme modèle, avec une génétique sophistiquée combinée à l’imagerie calcique à deux photons in vivo, à la biologie moléculaire et à l’analyse comportementale.
L’un de mes principaux centres d’intérêt consiste à déchiffrer le code neuronal qui représente les informations des signaux de valeurs dans le cerveau de la mouche. Ces informations sont essentielles pour prendre des décisions correctes basées sur les valeurs. Nous avons précédemment montré que de multiples types de récompenses et de punitions sont relayés par des ensembles spécifiques de neurones dopaminergiques qui assignent des valeur positifs ou négatifs au cours de l’apprentissage associatif. Ici, nous visons à examiner les circuits neuronaux qui représentent l’information de valeur que ces neurones dopaminergiques intègrent pour générer un signal de valeur.
Codage relatif de la valeur
Lors de l’apprentissage associatif, des valeurs absolues (bonne ou mauvaise) et/ou relatives (meilleur ou pire que) peuvent être attribuées à chaque expérience et peuvent être utilisées ultérieurement pour guider un comportement approprié. Mes travaux antérieurs ont montré que les neurones dopaminergiques qui relaient la récompense sont essentiels pour comparer les expériences aversives différentes et pour attribuer une valeur relative aversive aux stimuli au cours de l’apprentissage associatif (Perisse et al., 2013). Nos travaux récents (Villar et al., 2022) et d’autres de la littérature ont proposé que les interactions entre les systèmes appétitif et aversif sont essentielles pour signaler la valeur absolue des stimuli au cours de l’apprentissage et pour réévaluer les informations apprises. En revanche, la manière dont ces systèmes interagissent et opèrent au niveau de ces interactions pour coder la valeur relative n’est pas bien comprise. Nous étudions donc les circuits et mécanismes neuronaux impliqués dans la comparaison des expériences de valeur apprise pendant l’apprentissage, nécessaire pour générer un signal de valeur relative qui est attribué aux stimuli sensoriels (ici les odeurs) pendant l’apprentissage.
Décisions basées sur la valeur
Pour survivre, les animaux doivent souvent comparer et choisir entre plusieurs options en fonction de la valeur attribuée à chacune d’entre elles au cours de leurs expériences passées. La manière dont les mouches utilisent les informations de valeurs apprises pour sélectionner une action appropriée n’est pas encore claire. Nous avons précédemment identifié des circuits neuronaux spécifiques impliqués dans l’approche et l’évitement appris dans es mushroom body, une structure cérébrale centrale impliquée dans l’apprentissage, la mémoire et le comportement orienté vers un but. Nous cherchons à comprendre les mécanismes neuronaux qui sous-tendent la représentation de la valeur absolue et/ou relative apprise nécessaire pour sélectionner une action appropriée lors de choix basés sur la valeur.
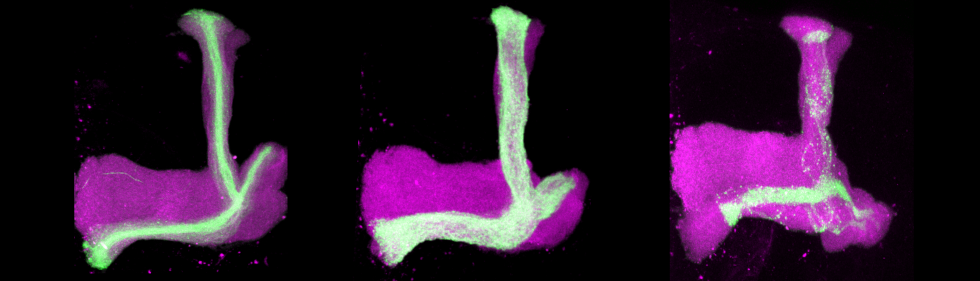
Mushroom body (magenta) et sous-types αβ (vert)

 IGF Nord 003
IGF Nord 003 04 34 35 93 47
04 34 35 93 47
 IGF Nord 003
IGF Nord 003 04 34 35 93 46
04 34 35 93 46
 IGF Nord 003
IGF Nord 003 04 34 35 93 46
04 34 35 93 46
 IGF Nord 003
IGF Nord 003 04 34 35 93 46
04 34 35 93 46
 IGF Nord 003
IGF Nord 003 04 34 35 93 47
04 34 35 93 47- Perisse E, Miranda M, Trouche S. Modulation of aversive value coding in the vertebrate and invertebrate brain. Curr Opin Neurobiol. 2023 Apr;79:102696. doi: 10.1016/j.conb.2023.102696.
- Villar ME, Pavão-Delgado M, Amigo M, Jacob PF, Merabet N, Pinot A, Perry SA, Waddell S, Perisse E. Differential coding of absolute and relative aversive value in the Drosophila brain. Curr Biol. 2022 Nov 7;32(21):4576-4592.e5. doi: 10.1016/j.cub.2022.08.058.
- Felsenberg J, Jacob PF, Walker T, Barnstedt O, Edmondson-Stait AJ, Pleijzier MW, Otto N, Schlegel P, Sharifi N, Perisse E, Smith CS, Lauritzen JS, Costa M, Jefferis GSXE, Bock DD, Waddell S. Integration of Parallel Opposing Memories Underlies Memory Extinction. 2018 Oct 18;175(3):709-722.e15. doi: 10.1016/j.cell.2018.08.021.
- Perisse E, Owald D, Barnstedt O, Talbot CB, Huetteroth W, Waddell S. Aversive Learning and Appetitive Motivation Toggle Feed-Forward Inhibition in the Drosophila Mushroom Body. 2016 Jun 1;90(5):1086-99. doi: 10.1016/j.neuron.2016.04.034.
- Owald D, Felsenberg J, Talbot CB, Das G, Perisse E, Huetteroth W, Waddell S. Activity of defined mushroom body output neurons underlies learned olfactory behavior in Drosophila. 2015 Apr 22;86(2):417-27. doi: 10.1016/j.neuron.2015.03.025.
- Huetteroth W, Perisse E, Lin S, Klappenbach M, Burke C, Waddell S. Sweet taste and nutrient value subdivide rewarding dopaminergic neurons in Drosophila. Curr Biol. 2015 Mar 16;25(6):751-758. doi: 10.1016/j.cub.2015.01.036.
- Das G, Klappenbach M, Vrontou E, Perisse E, Clark CM, Burke CJ, Waddell S. Drosophila learn opposing components of a compound food stimulus. Curr Biol. 2014 Aug 4;24(15):1723-30. doi: 10.1016/j.cub.2014.05.078.
- Perisse E, Yin Y, Lin AC, Lin S, Huetteroth W, Waddell S. Different Kenyon cell populations drive learned approach and avoidance in Drosophila. 2013 Sep 4;79(5):945-56. doi: 10.1016/j.neuron.2013.07.045.
- Burke CJ, Huetteroth W, Owald D, Perisse E, Krashes MJ, Das G, Gohl D, Silies M, Certel S, Waddell S. Layered reward signalling through octopamine and dopamine in Drosophila. 2012 Dec 20;492(7429):433-7. doi: 10.1038/nature11614.
- Perisse E, Raymond-Delpech V, Néant I, Matsumoto Y, Leclerc C, Moreau M, Sandoz JC. Early calcium increase triggers the formation of olfactory long-term memory in honeybees. BMC Biol. 2009 Jun 16;7:30. doi: 10.1186/1741-7007-7-30.
• 2023 : Emma Delon (Licence), Université de Nîmes, France.
• 2023 : Hadi-Abdul Al-Hasan (Master 2), Université de Strasbourg, France.
• 2023 : Clara Guiraud (Master 1), Université de Montpellier, France.
• 2023 : Margaux Vieu (Licence), Université de Nîmes, France.
• 2022 : Anh-Kiet Truong (Master 1), Université de Montpellier, France.
• 2022 : Danaë Ajas (Master 1), Université de Montpellier, France.
• 2021-2022 : Nesrine Merabet (IE), Inserm, France.
• 2021 : Marie Amigo (Master 2), Université de Montpellier, France.
• 2021 : Elsa Karam (Master 1), Université de Montpellier, France.
• 2021 : Thibaut Allenbach (Licence), Université de Nimes, France.
• 2020 : Cynthia Lelievre (Licence), Université de Nimes, France.
• 2020 : Hadrien Plat (Master 1), Université de Montpellier, France.
• 2020 : Laura Abate (Master 1), Université de Montpellier, France.
• 2020 : Theo Urgin (Master 2), Université de Montpellier, France.
• 2020 : Julie Beauduffe (Master 2), Université de Toulouse, France.
• 2019 : Victoria Breinlen (Licence), Université de Montpellier, France.
• 2019 : Maxime Verdy (Master 1), Université de Montpellier, France.
• 2019 : Jamie Bride (Master 1), Université de Montpellier, France.
• 2019 : Laetitia Peurien (Master 2), Université de Montpellier, France.
• 2019-2021 : Miguel Delgado (IE), Inserm, France.
• 2019-2021 : Maria-Eugenia Villar (Postdoc), Inserm, France.






