Équipe Julie PANNEQUIN
Signalisation, Plasticité et Cancer
Projet Surveillance de l’ADN tumoral circulant (ADNct) pour l’analyse des récidives du cancer colorectal
RESPONSABLE

Personnel IGF impliqué
Julie PANNEQUIN
DR2, CNRS
Jean-Marc PASCUSSI
CRCN, Inserm
Caroline BONNANS
CRCN, Inserm
Jihane VITRE BOUBAKER
Thèse CNRS
Szimonetta HIDEG
AJT CDD, UM
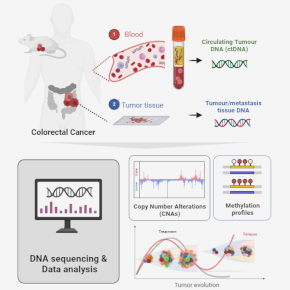
Notre groupe se consacre à l’étude de la progression et de la récurrence du cancer colorectal (CCR) en analysant des données de séquençage génomique provenant d’échantillons cliniques et de modèles précliniques. Nous proposons une recherche interdisciplinaire combinant la bioinformatique, la recherche expérimentale et translationnelle afin de développer de nouvelles méthodes analytiques pour mieux comprendre la dynamique génomique du CCR et améliorer le suivi clinique de ces tumeurs.
La récidive tumorale et les métastases sont les principales causes de mortalité du cancer colorectal (CCR), affectant près de la moitié des patients dans les 5 ans suivant un traitement à visée curative. Le CCR récidivant peut, dans un premier temps, ne pas être détecté par la surveillance standard, ce qui souligne la nécessité d’une surveillance accrue pour identifier les patients présentant une maladie résiduelle minimale (MRD) après traitement. L’ADN tumoral circulant (ADNct) mesuré par biopsies liquides est une approche non invasive prometteuse pour le suivi continu des patients, avec une sensibilité plus élevée que l’imagerie conventionnelle, permettant une meilleure détection de la dormance tumorale, de la rechute et de la résistance thérapeutique. Cependant, son analyse est extrêmement difficile en raison de la faible fraction d’ADN cellulaire dérivé de la tumeur, et il n’y a pas encore de consensus sur sa validité clinique dans le cancer colorectal. Malgré les progrès réalisés, le séquençage de nouvelle génération (NGS), qui est l’étalon-or actuel, présente toujours une sensibilité limitée, en particulier en cas de rémission après traitement. En outre, il nécessite beaucoup de ressources et n’est pas toujours accessible sur le plan clinique.
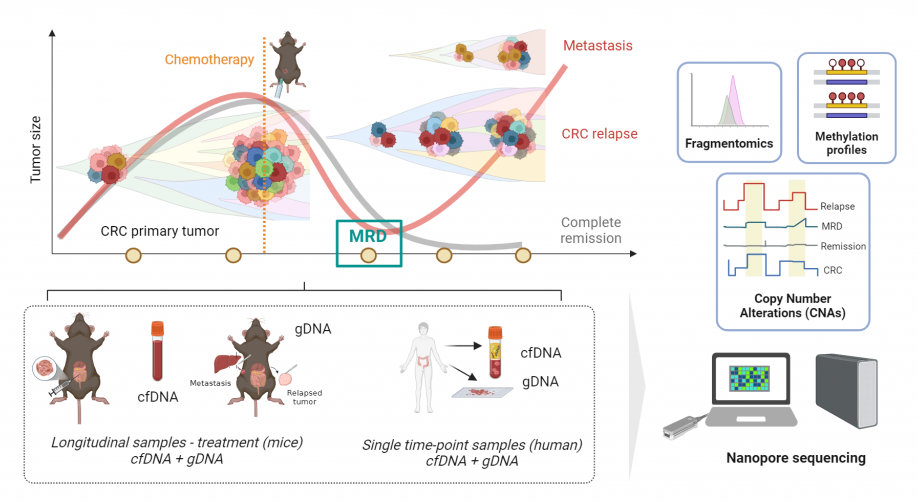
Ici, notre objectif principal est d’améliorer la détection de la progression et de la récidive du CCR en développant une stratégie de surveillance peu invasive, personnalisée et rentable basée sur l’analyse multimodale de l’ADNct à partir d’un seul échantillon de sang. En exploitant le potentiel du séquençage par nanopores de troisième génération (nanopore sequencing), notre approche vise à augmenter la sensibilité de la détection de l’ADNct, en particulier lorsqu’il est présent à des niveaux minimaux après le traitement (MRD), ce qui peut être considéré comme un marqueur de récidive précoce et de résistance thérapeutique.
Pour atteindre cet objectif, le projet comprend :
– l’utilisation de modèles de souris pour modéliser les schémas cliniques de progression tumorale et de résistance thérapeutique
– L’utilisation d’échantillons de CCR provenant de biopsies de plasma et de tissus de patients
– Le développement de méthodes informatiques pour l’analyse multimodale de l’ADNct à partir de données de séquençage par nanopore.
Principales publications
• Pedrola A et al. (2022) Bioinformatics. 38(8):2374-2376.
• Yngvadottir B, Andreou A, Bassaganyas L, et al. (2022) Hum Mol Genet. 31(17):3001-3011
• Franch-Expósito S, Bassaganyas L, et al. (2020) Elife. 9:e50267
• Bassaganyas L, Pinyol R, Esteban-Fabró R, et al. (2020). Clin Cancer Res 26(23):6350-6361
• Pinyol R, Montal R, Bassaganyas L, et al. (2019) Gut. 68(6):1065-1075
• Bassaganyas L, Freedman G, et al. (2018) Hum Mutat. 39(1):167-171
• Bassaganyas L et al. (2013) Leukemia. 27(12):2376-2379
• Escaramís G, Tornador C, Bassaganyas L, et al. (2013) PLoS One. 8(5):e63377.
• Puente XS, et al. (2011) Nature. 475(7354):101-105


