Équipe Philippe MARIN
Neuroprotéomique et signalisation des pathologies cérébrales
Projet Trafic protéique et maladies neurodégénératives
RESPONSABLE

Personnel IGF impliqué
Marie-Laure PARMENTIER
DR2, Inserm
Sylvie CLAEYSEN
CRHC, Inserm
Philippe MARIN
DR1, CNRS
Aurore FILAQUIER
Thèse, UM
Éloïse NEEL
Doctorante CNRS
Morgane DENUS
IE, CDD CNRS
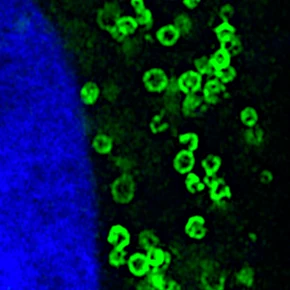
L’accumulation de protéines mal-conformées, telles que les protéines Tau et l’alpha-synucléine (α-Syn), constitue une caractéristique pathologique partagée par plusieurs maladies neurodégénératives, notamment la maladie d’Alzheimer (AD) et la maladie de Parkinson (PD). Jusqu’à récemment, il était admis que l’accumulation de Tau et de l’α-Syn se produisait de manière cellulaire-autonome. Cependant, des recherches récentes suggèrent maintenant qu’elles se propagent comme des prions en étant libérées des cellules via un mécanisme de sécrétion non conventionnelle (UPS pour Unconventional Protein Secretion), c’est-à-dire indépendamment de la voie de sécrétion réticulum endoplasmique-appareil de Golgi.
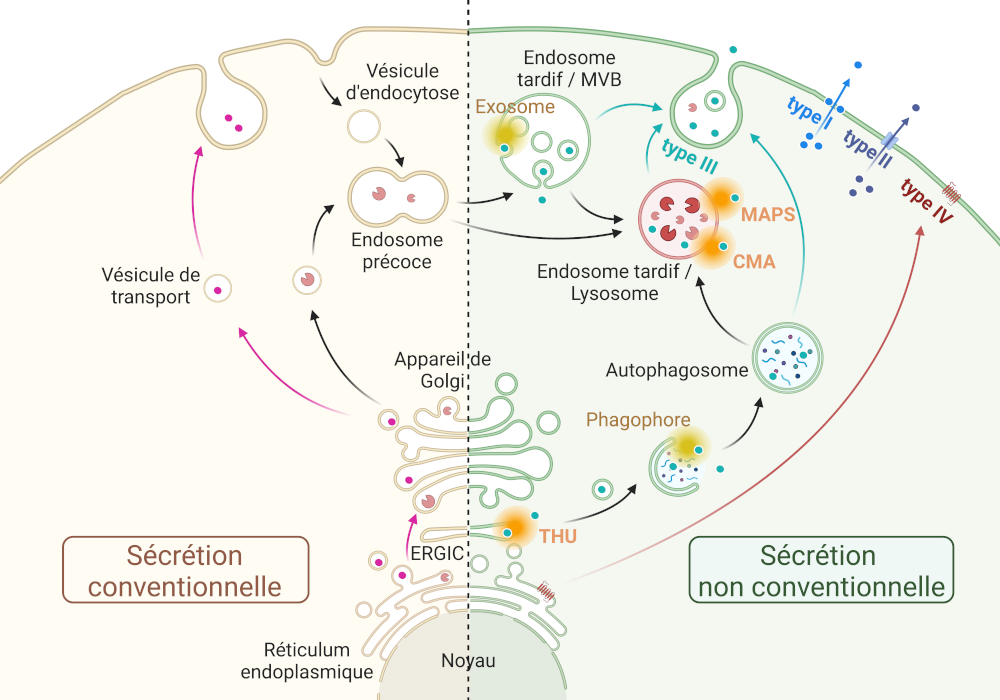
Nous avons récemment mis en évidence le rôle crucial des lysosomes dans le processus d’UPS, notamment dans la propagation de Tau et de l’α–Syn par exocytose lysosomale. Ces résultats nous ont conduit à formuler l’hypothèse selon laquelle, en réponse à un stress protéotoxique, les lysosomes pourraient être remodelés et/ou détournés pour le transport et la sécrétion. En effet, en plus de leur fonction dégradative, les lysosomes sont des structures très dynamiques dotées de multiples propriétés biologiques, pouvant fusionner avec la membrane plasmique après transport le long des microtubules. Des données récentes ont également lié le développement de plusieurs maladies neurodégénératives à des défauts dans les processus de dégradation lysosomale. Dans ce contexte, un défi majeur consiste à comprendre comment les lysosomes sont détournés de leur fonction dégradative et acquièrent des fonctions de transport/sécrétion favorisant la dissémination de Tau et de l’α–Syn. Il est également crucial d’explorer si la compréhension mécanistique de ces processus pourrait jeter les bases de nouvelles stratégies thérapeutiques et diagnostiques pour les maladies neurodégénératives.
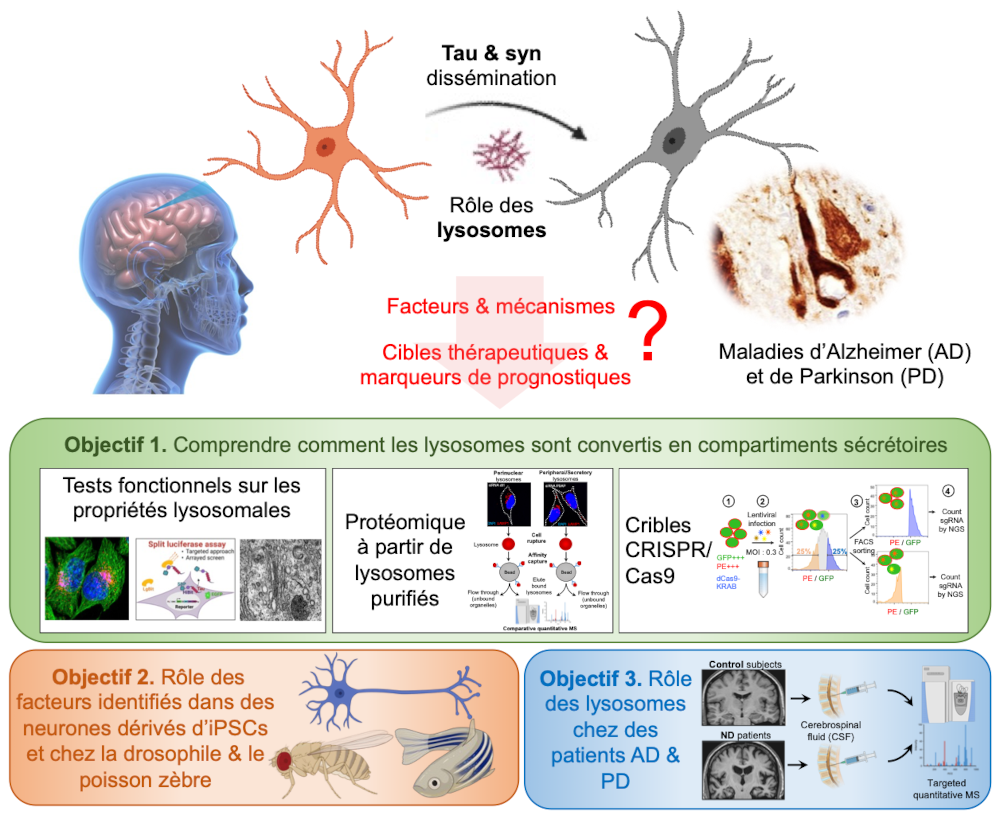
Dans le cadre de notre projet, nous développons des approches multidisciplinaires et translationnelles pour étudier le rôle des lysosomes dans les maladies neurodégénératives. Plus précisément, notre projet vise à :
- Identifier les acteurs moléculaires activés ou recrutés dynamiquement au niveau des lysosomes pour les détourner en compartiments essential au processus d’UPS, et identifier les facteurs impliqués à chaque étape du trafic de Tau et de l’α-Syn. A cette fin, nous utilisons des tests cellulaires innovants basés sur la technologie split luciférase et le système RUSH, ainsi que des outils développés récemment, tels que des tests fonctionnels sur les propriétés lysosomales, une plateforme pour des cribles génétiques CRISPR/cas9 réalisés sous forme de pool à l’échelle du génome entier, et des approches de protéomique à partir de lysosomes purifiés.
- Évaluer le rôle des facteurs identifiés dans les neurones dérivés de sujets sains et de patients atteints de AD/PD à partir de cellules souches pluripotentes induites. Nous étudions également leur impact dans des modèles in vivo tels que la drosophile et le poisson-zèbre, afin de valider leur pertinence physiopathologique et révéler leur potentiel thérapeutique.
- Examiner la pertinence du rôle des lysosomes en tant qu’organelles impliquées dans la dissémination de Tau et de l’α–Syn chez les patients atteints de maladies neurodégénératives. Nous évaluons les quantités d’enzymes/facteurs lysosomaux à partir d’échantillons de liquide céphalorachidien en utilisant des approches de spectrométrie de masse ciblée. En plus de confirmer notre modèle à l’aide d’échantillons cliniques, cela pourrait conduire à l’identification de nouveaux biomarqueurs pour les maladies neurodégénératives.
Ce projet, au carrefour de nombreux défis, pourrait permettre des avancées majeures dans la compréhension des mécanismes fondamentaux régissant la biologie des lysosomes. De plus, il pourrait avoir un impact important dans la recherche biomédicale en ouvrant la voie au développement de nouvelles stratégies thérapeutiques et diagnostiques pour certaines maladies neurodégénératives.
Principales publications
• Filaquier A., et al. (2022) Curr Opin Cell Biol, 16;75:102072.
• Stamatakou E., et al. (2020) Cell Discovery, 10.1038/s41421-020-0158-y
• Bassaganyas L., et al. (2019) J Cell Biol, 11:3861-3879.
• Villeneuve J., et al. (2018) J Cell Biol, 2:649-665.
• Villeneuve J., et al. (2017) Mol Biol Cell, 1;28(1) :141-151
• Villeneuve J., et al. (2013) Embo J, 1:72-85.
Financements
• 2024-2027 Fondation pour la Recherche Médicale (FRM) – Partenaire
• 2023-2027 ANR 2023 UnProSec – Coordinateur
• 2023-2025 Fondation pour la Recherche sur le Cerveau (FRC) – Coordinateur
• 2023-2025 Association France Alzheimer – Investigateur Principal
• 2022-2024 Fondation Vaincre Alzheimer – Investigateur Principal
• 2021-2023 Association France Parkinson – Investigateur Principal
Collaborations
• Yoan Arribat (IRMB, Montpellier)
• Laia Bassaganyas (IGF, Montpellier)
• Ana Boulanger (IGH, Montpellier)
• Carole Crozet (INM, Montpellier)
• Sylvain Lehmann (CHU, Montpellier)
• Mireille Rossel (MMDN, Montpellier)
• Chiara Zurzolo (Pasteur, Paris)
Alumni
• William Fargues (Master & Engineer, 2023-2024)
• Adrià Martinez (Master, 2023)
• Amélie Vidal (Master, 2023)
• Lola ARGENSON (Master, 2022)
• Ariane BROWER (Master, 2022)
• Elisa GARBAYE (Master, 2022)


