Équipe Philippe MARIN
Neuroprotéomique et signalisation des pathologies cérébrales
Projet Microbiote, sérotonine et maladies neurodégénératives
RESPONSABLE

Personnel IGF impliqué
Philippe MARIN
DRCE, CNRS
Joël BOCKAERT
PU, UM
Marie-Laure PARMENTIER
DR2, Inserm
Sylvaine ARTERO
CRCN, Inserm
Lucy KUNDURA
Post-doc, Inserm
Thomas CUREL
Doctorant, Inserm
Sonya GALANT
IECN, CNRS
S’appuyant sur une expertise en neuropharmacologie des récepteurs aux protéines G (RCPG) et plus particulièrement des récepteurs de la sérotonine (5-HT), mais également sur des travaux précurseurs sur le microbiote intestinal, ce groupe de recherche vise à proposer des innovations thérapeutiques face aux maladies neurodégénératives et plus particulièrement de la maladie d’Alzheimer. Cet objectif se découpe en 3 axes :
Protéome du récepteur 5-HT4 et prévention de la maladie d’Alzheimer
Ligands multi-cibles innovants dans le contexte de la maladie d’Alzheimer
Protéome du récepteur 5-HT4 et prévention de la maladie d’Alzheimer
Notre objectif est de développer une nouvelle approche thérapeutique visant à augmenter le clivage de l’APP par l’α-sécrétase ADAM10 afin de contrebalancer la maturation de l’APP vers la voie non-amyloïdogène.
Notre outil principal est le récepteur de la sérotonine de type 4 (5-HT4) qui nous permet de :
- Favoriser le trafic intracellulaire de l’a-sécrétase ADAM10 vers la membrane plasmique où elle est active
- Stimuler l’ADAM10 et la production du fragment soluble sAPPa aux propriétés neuroprotectrices
- Rechercher par protéomique de nouveaux partenaires protéiques qui agissent sur le trafic et/ou le métabolisme de l’APP.
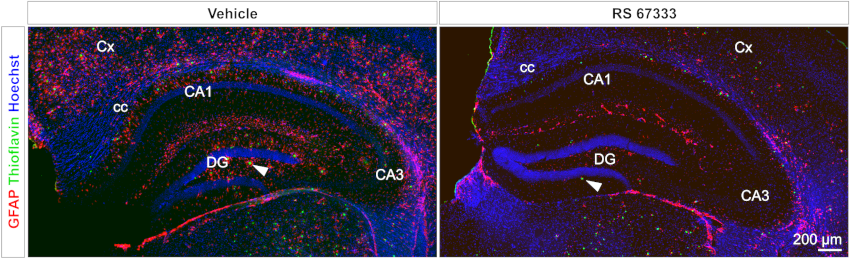
Réduction de l’amyloïdose et de l’astrogliose par activation du récepteur 5-HT4.
Modèle murin 5xFAD traité au RS 67333 (agoniste R5-HT4). Plaques amyloïdes (Thioflavine T, vert). Astrocytes (GFAP, rouge). Tiré de Giannoni P. Front Aging Neurosci. 2013.
Principales publications
• Giannoni P., et al. (2020) Front Aging Neurosci, 12, 3.
• Baranger K., et al. (2017) Neuropharmacology, 126, 128-141.
• Giannoni P., et al. (2016) Neurobiol Dis, 88, 107-17.
• Arango-Lievano M., et al. (2016) J Vis Exp, 6, 54796.
• Saraceno C., et al. (2014) Cell Death Dis, 5, e1547.
• Giannoni P., et al. (2013) Front Aging Neurosci, 5, 96.
• Cochet M., et al. (2013) ACS Chem Neurosci, 4, 130-40.
Financements
• 2015-2018 Fédération pour la Recherche sur le Cerveau (FRC 2015) – Partenaire
• 2013-2018 ANR 2012-ADAMGUARD – Responsable de tâche
• 2012-2015 Région Languedoc Roussillon – Investigateur Principal
• 2011-2014 Association France Alzheimer – Investigateur Principal
Collaborations
• Stephan Lichtenthaler (DZNE, Munich)
• Monica Di Lucca (Milan)
• Santiago Rivera (Marseille)
• François Roman (Marseille)
• Nicola Marchi (Montpellier)
• Freddy Jeanneteau (Montpellier)
Alumni
• Hugo Payan (Doctorat, 2016-2020)
• Patrizia Giannoni (Post-Doc., 2011-2016)
• Florence Gaven (IE, 2003-2015)
• Romain Donneger (Doctorat, 2010-2014)
• Elena Marcello (Post-Doc., 2011-2012)
• Maud Cochet (Doctorat, 2007-2011)
Ligands multi-cibles innovants dans le contexte de la maladie d’Alzheimer
Notre consortium propose de concevoir des agents thérapeutiques de type « ligands multi-cibles » (MTDL, Multi-Targeted Directed Ligands) capables d’engager plusieurs acteurs moléculaires impliquées dans la pathogenèse de la maladie afin d’obtenir une combinaison d’effets symptomatiques, procognitifs et impactant l’évolution de la maladie d’Alzheimer.
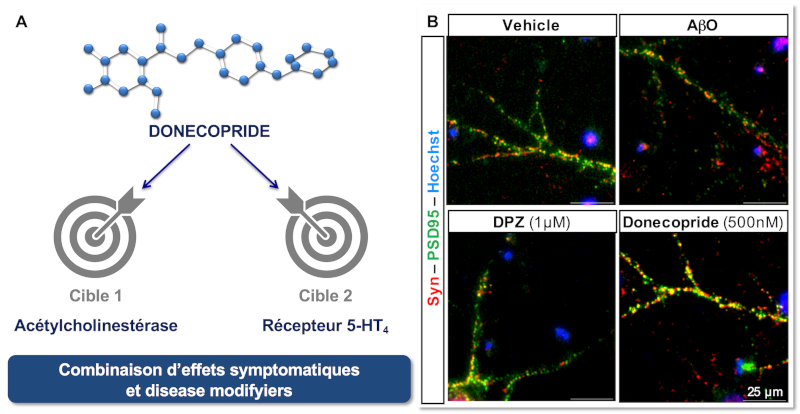
Conception et caractérisation du donécopride
A. Candidat médicament présentant à la fois une activité inhibitrice de l’acétycholinestérase et un profil agoniste du récepteur 5-HT4 conduisant à un effet procognitif in vivo en modèle murin.
B. Neurones primaires d’hippocampe de rat en présence du véhicule, d’oligomères d’Aβ (AβO), de donepezil (DPZ) ou du donécopride. Synaptophysine (rouge), PSD95 (vert), Hoechst (bleu). Tiré de Rochais C. Br J Pharmacol, 2020.
Principales publications
• Antonijevic M., et al. (2024) Molecules, 29, 515.
• Toublet F. X., et al. (2021) Eur J Med Chem. 210, 113059.
• Lalut J., et al. (2020) Sci Rep, 10, 314.
• Toublet F. X., et al. (2019) Molecules, 24.
• Rochais C., et al. (2020) Br J Pharmacol, 177, 1988-2005
• Lanthier C., et al. (2019) Eur J Med Chem, 182, 111596.
• Hatat B., et al. (2019) Front Aging Neurosci. 11,148.
• Rochais C., et al. (2015) J Med Chem, 58, 3172-87.
• Lecoutey C., et al. (2014) PNAS, 111, E3825-30.
Financements
• 2020-2025 ANR 2020-DOWNALZ – Partenaire
• 2016-2019 Ligue Européenne Contre La Maladie d’Alzheimer (LECMA) – Coordinateur
• 2015-2018 Fondation Plan Alzheimer (AAP 2015) – k€100 (k€33) – Partenaire
• 2012-2014 Ligue Européenne Contre La Maladie d’Alzheimer (LECMA) – Coordinateur
Collaborations
• Patrick Dallemagne (Caen)
• Michel Boulouard (Caen)
• Santiago Rivera (Marseille)
Alumni
• Caroline Ismeurt (Thèse, 2017-2021)
• Bérénice Hatat (Thèse, 2016-2019)
• Hugo Payan (Thèse, 2016-2020)
• Patrizia Giannoni (Post-Doc., 2011-2016)
• Florence Gaven (IE, 2003-2015)
Brevets
• Dallemagne P., Rochais C. & Claeysen S. EP 3628660, 2020
• Dallemagne P., Rochais C. & Claeysen S. EP 3628315, 2020
• Dallemagne P., Rochais C. & Claeysen S. WO 2020065028, 2020
• Dallemagne P., Rochais C. & Claeysen S. WO 2020064979, 2020
Microbiote intestinal et maladie d’Alzheimer
Une dysbiose du microbiote intestinal jouerait un rôle central dans le phénomène inflammatoire chronique participant à la progression de la maladie d’Alzheimer. La formation de composés métaboliques par certaines bactéries influencerait les cellules immunitaires périphériques promouvant une inflammation systémique et au niveau central.
Notre objectif est de déterminer l’impact du microbiote intestinal sur le développement de la maladie d’Alzheimer afin de proposer des biomarqueurs d’origine bactérienne et des stratégies d’intervention innovantes basées sur une restauration de la composition du microbiote intestinal.

L’étude clinique MICMALZ NCT04841135 vise à :
- Caractériser la signature bactérienne sanguine et intestinale de patients Alzheimer et rechercher des biomarqueurs dérivés du microbiote
- Définir l’influence de la dysbiose intestinale de patients Alzheimer sur la cognition et l’évolution de la pathologie par transfert de microbiote en modèle murin de maladie d’Alzheimer

Le projet DENTALCOG ANR-22-CE36-0003 vise à :
- Analyser dans deux cohortes complémentaires en population générale les interrelations entre consommation des glucides raffinés, maladies parodontales et processus cognitifs, ainsi que les changements associés des biomarqueurs cérébraux et plasmatiques.
- Valider les résultats épidémiologiques et décrypter dans un modèle animal (souris 5xFAD) l’impact d’une consommation excessive de sucrose sur la parodontite, la cognition et le microbiote buccal.
Financements
• 2023-2026 ANR 2022-DENTALCOG– Partenaire
• 2021-2024 Programme Transversal INSERM MICROBIOTE 2 – Partenaire
• 2019-2022 Projet MICMALZ, Région Occitanie/FEDER – Coordinateur
• 2017-2020 Programme Transversal INSERM MICROBIOTE 1 – Partenaire
Collaborations
• Audrey Gabelle (CHU, Montpellier)
• Karim Bennys (CHU, Montpellier)
• Germain Busto (CHU, Montpellier)
• Yves Dauvilliers (CHU, Montpellier)
• Sylvain Lehmann (CHU, Montpellier)
• Xavier Collet (CREFRE, Toulouse)
• Damien Rei (NBX Biosciences, Montpellier)
• Sylvaine Artero (IGF, Montpellier)
• Michel Neunlist & Moustapha Cissé (Nantes)
• Samuel Chaffron (Nantes)
• Agnes Lehuen (Cochin, Paris)
• Sylvie Rabot (INRAE, Jouy-en-Josas)
• Christophe Junot (METABOHUB, CEA)
• Société MaaT Pharma (Lyon)
• Société VAIOMER (Labège)
Alumni
• Linda-Nora Mekki (IE, 2020-2022)
• Caroline Ismeurt (Thèse, 2017-2021)
• Patrizia Giannoni (Post-Doc., 2011-2016)
• Florence Gaven (IE, 2003-2015)


