Équipe Laurent JOURNOT
Génomique fonctionnelle des gènes soumis à empreinte parentale
Projet Caractérisation fonctionnelle du facteur de transcription ZAC1/PLAGL1
RESPONSABLES
Annie VARRAULT
CR CNRS

Laurent JOURNOT
DR CNRS
Personnel IGF impliqué
Anne LE DIGARCHER
AI CNRS
Tristan BOUSCHET
CR INSERM

Nous avons initialement cloné le ZAC1 murin et humain en tant que facteur de transcription à doigt de zinc qui induit l’apoptose et l’arrêt du cycle cellulaire dans différents types de cellules (Spengler et al., EMBO J, 1997 ; Varrault et al., Proc Natl Acad Sci USA, 1998 ; Pagotto et al., Endocrinology, 1999 ; Bilanges et al., Oncogene, 2001). Abdollahi et ses collaborateurs ont indépendamment cloné l’orthologue du rat qu’ils ont appelé Lot1 car son expression était perdue lors de la transformation des cellules épithéliales ovariennes du rat (Abdollahi et al., Cancer Res, 1997 ; Abdollahi et al., Oncogene, 1999). Il s’est avéré par la suite que ZAC1/LOT1 faisait partie d’une famille de trois gènes de protéines à doigt de zinc comprenant PLAG1-Pleomorphic adenoma gene 1, PLAGL2 et ZAC1/LOT1/PLAGL1.
ZAC1 est-il le gène suppresseur de tumeur en 6q24 ?
Compte tenu de ses propriétés fonctionnelles, de son inhibition au cours de la transformation épithéliale et de sa localisation chromosomique sur 6q24, une région connue pour abriter un gène suppresseur de tumeur, ZAC1 a été suggéré comme étant le gène suppresseur de tumeur 6q24. Aucune mutation inactivante n’a été identifiée à ce jour, mais une perte d’expression de ZAC1 a été observée dans divers néoplasmes (par exemple, Abdollahi et al, Oncogene, 1997 ; Varrault et al, Proc Natl Acad Sci USA, 1998 ; Bilanges et al., Oncogene, 1999 ; Pagotto et al., Cancer Res, 2000 ; Abdollahi et al., J Biol Chem, 2003 ; Kamikihara et al., Int J Cancer, 2005 ; Basyuk et al., Mol Cancer Res, 2005). Nous avons ensuite montré que l’inactivation constitutive de Zac1 chez la souris n’entraînait pas la formation de tumeurs (Varrault et al., Dev Cell, 2006). Ainsi, deux décennies après son clonage, il n’est toujours pas clair si ZAC1 est le gène suppresseur de tumeur en 6q24.
ZAC1 est le gène du DNT
Contrairement à la perte de fonction de ZAC1, le gain de fonction de ZAC1 par surexpression est clairement lié à un état pathologique. La démonstration est venue de deux lignes d’investigation indépendantes ; 1) la découverte que ZAC1 est imprimé maternellement (Piras et al., Mol Cell Biol, 2000 ; Arima et al., Genomics, 2000), et 2) la recherche du gène imprimé du diabète néonatal transitoire (DNT) en 6q24 (Kamiya et al., Hum Mol Genet, 2000 ; Docherty et al., Diabetologia, 2010). À cet égard, nous avons élucidé le mécanisme d’empreinte de ZAC1 en montrant que ZAC1 est imprimé maternellement, exprimé paternellement par la méthylation constitutive de son promoteur maternel (Varrault et al., J Biol Chem, 2001).
Les formes néonatales de diabète offrent la possibilité de découvrir des gènes importants pour le développement. Le diabète néonatal (DN) est un diabète monogénique qui englobe deux conditions distinctes, les formes transitoires (DNT) et permanentes (DNP) ; les deux conditions sont rares (Grulich-Henn et al., Diabet Med, 2010 ; Iafusco et al., Acta Diabetol, 2012).
Dans le DNP, l’insuffisance de sécrétion d’insuline survient à la fin de la période fœtale ou au début de la période post-natale et ne connaît pas de rémission. Les gènes mutés dans le DNP comprennent KCNJ11 et ABCC8, qui codent respectivement pour le récepteur 1 de la sulfonylurée (SUR1) et la sous-unité KIR6.2 du canal potassique sensible à l’ATP des cellules β. Par ailleurs, les patients atteints de DNP présentent des mutations des gènes INS, GCK ou PDX1.
Dans le cas du DNT, les patients sont plus jeunes au moment du diagnostic du diabète et ont des besoins initiaux en insuline plus faibles. Ils sont plus susceptibles d’avoir un retard de croissance intra-utérin et moins susceptibles de développer une acidocétose que les patients atteints de DNP. Un chevauchement considérable se produit entre les deux conditions, de sorte que le DNT ne peut pas être distingué du DNP sur la base des caractéristiques cliniques au début (Busiah et al., Lancet Diabetes Endocrinol, 2013). Au moins 85 % des patients atteints de DNT rechutent pendant l’adolescence et souffrent d’un diabète permanent (Busiah et al., Lancet Diabetes Endocrinol, 2013). Environ 25 % des patients atteints de DNT présentent des mutations dans les gènes KCNJ11 ou ABCC8. La majorité des patients atteints de DNT (75 %) présentent un défaut d’empreinte ou un défaut cytogénétique de la région chromosomique 6q24 (Temple & Shield, J Med Genet, 2002). La région critique DNT 6q24 abrite un gène à empreinte maternelle et à expression paternelle, ZAC1/PLAGL1, qui est le gène candidat DNT 6q24 (Docherty et al., Diabetologia, 2010). Les patients atteints de DNT 6q24 ont deux allèles ZAC1 actifs, résultat de trois mécanismes possibles (Figure 1). Nos travaux actuels visent à élucider les mécanismes par lesquels le double dosage de ZAC1 altère le développement et/ou la fonction des cellules β pancréatiques.
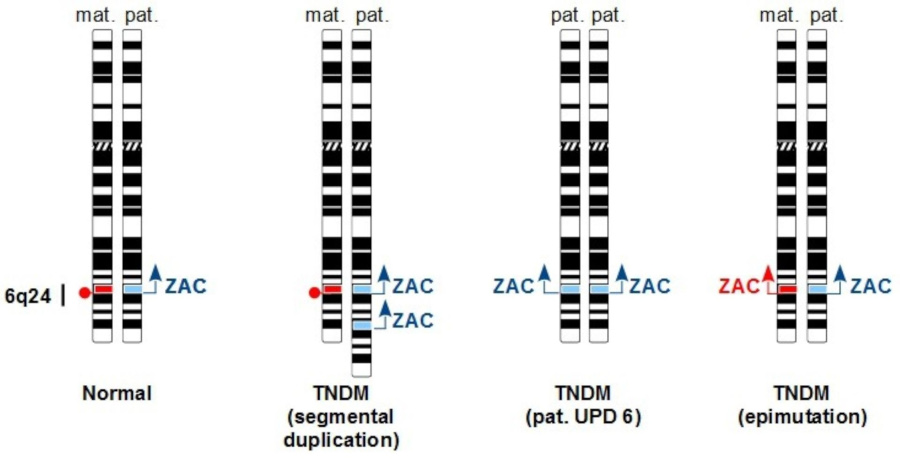
Cytogénétique moléculaire du DNT 6q24. Contrairement aux contrôles sains, les patients atteints de DNT possèdent deux allèles de ZAC1 actifs, résultant de l’un des trois mécanismes possibles suivants : 1) duplication segmentaire du 6q24 paternel ; 2) disomie uniparentale du chromosome 6 paternel (pat. UPD 6) ; 3) hypo-méthylation du 6q24 maternel (épimutation).
Gènes cibles de Zac1
Plus récemment, nous avons cherché à identifier les gènes cibles de Zac1 à l’échelle du génome (Varrault et al., Nucleic Acids Res, 2017). Nous avons montré que l’augmentation de la régulation de Zac1 était associée à la sortie du cycle cellulaire physiologique qui se produisait avec l’inhibition du contact, le retrait des facteurs de croissance ou la différenciation cellulaire. Pour mieux comprendre le mécanisme d’action de Zac1, nous avons identifié ses gènes cibles en combinant l’immunoprécipitation de la chromatine et la transcriptomique à l’échelle du génome dans des lignées cellulaires transfectées. La régulation des gènes induite par Zac1 est corrélée à une liaison multiple à la région proximale du promoteur par l’intermédiaire d’un motif riche en GC. Les gènes cibles de Zac1 comprenaient de nombreux gènes impliqués dans la signalisation, l’adhésion cellulaire et la composition de la matrice extracellulaire, y compris les collagènes. Les cibles de Zac1 comprenaient également 22 % des 409 gènes qui composent le réseau de gènes à empreinte parentale (IGN). Dans l’ensemble, ces travaux ont permis d’identifier Zac1 comme un facteur de transcription qui coordonne la régulation d’un sous-ensemble de gènes de l’IGN et contrôle la composition de la matrice extracellulaire.
Principales publications
• Varrault A et al. (2017) Nucleic Acids Res, 45, 10466.
• Varrault A et al. (2006) Dev Cell, 11, 711.
• Basyuk E et al. (2005) Mol Cancer Res, 3, 483.
• Varrault A et al. (1998) Proc Natl Acad Sci USA, 95, 8835.
• Spengler D et al. (1997) EMBO J, 16, 2814.
Financements
• 2019-2021 Labex EpiGenMed-Partner
• 2007-2011 ANR 2007-EpiNet-Coordinator
Collaborations
• Myriam Cnop (Brussels)
• Robert Feil (Montpellier)
• Carol Schuurmans (Toronto)
Alumni
• Eugenia BASYUK (postodoc fellow, 2000-2002)


