Équipe Philippe JAY
Auto-renouvellement et différenciation des epithelia

Notre équipe étudie la fonction d’interface des epithelia gastriques et intestinaux entre notre organisme, le microbiome, et certains agents pathogènes. Notre objectif principal est de comprendre comment nous nous adaptons aux variations de notre environnement. En fonction de ces variations, nous analysons en particulier les modifications des fonctions de la muqueuse digestive, incluant les cellules souches épithéliales, le système immunitaire et certaines cellules immunomodulatrices nommées cellules tuft. Nos résultats permettent de mieux cerner les mécanismes clefs impliqués dans des maladies telles que les maladies inflammatoires chroniques, les infections par des agents pathogènes et le cancer, dans le but d’identifier de nouvelles opportunités thérapeutiques.
L’épithélium intestinal et gastrique est constitué d’une monocouche cellulaire représentant la principale interface entre notre organisme et son environnement. Le compartiment de la lamina propria, contigu à l’épithélium, contient de nombreuses cellules immunitaires chargées de contrôler la barrière intestinale, notamment contre des organismes pathogènes. Le maintien de l’homéostasie et la mise en place de réponses immunitaires appropriées reposent sur le dialogue des cellules immunitaires avec les cellules épithéliales en contact direct avec les micro-organismes de la lumière intestinale. Notre équipe étudie l’implication de ce dialogue dans différentes situations physiopathologies, notamment les infections, les maladies inflammatoires chroniques et le cancer.
Notre équipe, en même temps que d’autres, a récemment découvert la première fonction des cellules tuft de l’épithélium intestinal comme sentinelles capables d’identifier des dangers luminaux et d’initier des réponses immunitaires dans la lamina propria (Gerbe et al. Nature 2016), et plus récemment, leur dialogue avec les cellules de Paneth pour réguler le microbiote. (Coutry et al., 2023).
Les projets en cours ont pour objectifs de découvrir de nouvelles facettes de la fonction des cellules tuft, par exemple avec la production de molécules effectrices comme l’acetylcholine pour lutter contre les infections parasitaires. Nous recherchons aussi les mécanismes permettant aux cellules tuft de mettre en place un microenvironnement immunitaire délétère, facilitant l’émergence de maladies inflammatoires chronique ou l’initiation tumorale dans l’estomac et l’intestin.
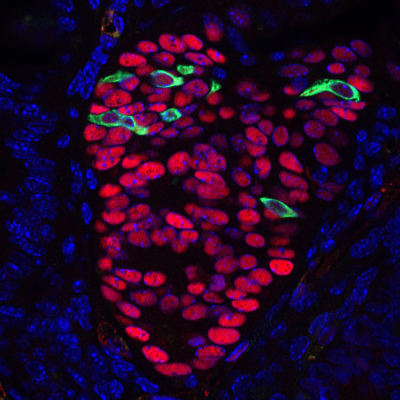
Présence de cellules tuft exprimant le marqueur Dclk1 (vert) dans les tumeurs intestinales de souris mises en évidence par l’expression ectopique du marqueur Sox17 (rouge). Les noyaux sont colorés au DAPI (bleu).

 IGF Nord 107b
IGF Nord 107b 04 34 35 92 98
04 34 35 92 98
 IGF Nord 121
IGF Nord 121 04 34 35 93 03
04 34 35 93 03
 IGF Nord 121
IGF Nord 121 04 34 35 93 03
04 34 35 93 03
 IGF Nord 103
IGF Nord 103 04 34 35 92 66
04 34 35 92 66
 IGF Nord 103
IGF Nord 103 04 34 35 92 66
04 34 35 92 66
 IGF Nord 103
IGF Nord 103 04 34 35 92 66
04 34 35 92 66
 IGF Nord 107b
IGF Nord 107b 04 34 35 92 98
04 34 35 92 98
 IGF Nord 103
IGF Nord 103 04 34 35 92 66
04 34 35 92 66
 IGF Nord 121
IGF Nord 121 04 34 35 93 03
04 34 35 93 03- Coutry N., Nguyen J., Soualhi S., Gerbe F., Meslier V., Dardalhon V., Almeida M., Quinquis B., Thirion F., Herbert F., Gasmi I., Lamrani A., Giordano A., Cesses P., Garnier L., Thirard S., Greuet D., Cazevieille C., Bernex F., Bressuire C., Winton D., Matsumoto I., Blottière H.M., Taylor N. and Jay P. Crosstalk between Paneth and tuft cells drives dysbiosis and inflammation in the gut mucosa. Proc Natl Acad Sci U S A 2023 Jun 20;120(25): e2219431120. doi: 10.1073/pnas.2219431120. PMID:
- Bas J., Jay P*. and Gerbe F.* Intestinal tuft cells, what else? Semin Cell Dev Biol. 2023 Dec : 150-151:35-42. doi: 10.1016/j.semcdb.2023.02.012. PMID. *: corresponding authors
- Bruschi M., Garnier L., Gerbe F., Cleroux E., Dumas M., Bardet A.F., Quesada S., Cesses P., Weber M. and Jay P. Loss of Apc rapidly impairs DNA methylation programs and cell fate decisions in Lgr5+ intestinal stem cells. Cancer Res. 2020 Jun 1;80(11):2101-2113. doi: 10.1158/0008-5472.CAN-19-2104. PMID: 32213541.
- Bornstein C., Nevo S., Giladi A., Kadouri N., Pouzolles M., Gerbe F., David E., Machado A., Chuprin A., Toth B., Goldberg O., Itzkovitz S., Taylor N., Jay P., Zimmermann V., Abramson J. and Amit I. Single cell mapping of the thymic stroma identifies IL25-producing tuft epithelial cells. Nature 2018 Jul;559(7715):622-626. doi: 10.1038/s41586-018-0346-1. PMID: 30022162.
- Gerbe F. and Jay P. Intestinal tuft cells: epithelial sentinels linking luminal cues to the immune system. Mucosal Immunol. 2016 Nov;9(6):1353-1359. doi: 10.1038/mi.2016.68. PMID: 27554294.
- Gerbe F., Sidot E., Smyth D. J., Ohmoto M., Matsumoto I., Dardalhon V., Cesses P., Garnier L., Pouzolles M., Brulin B., Bruschi M., Harcus Y., Zimmermann V. S., Taylor N., Maizels M. and Jay P. Intestinal epithelial tuft cells initiate type 2 mucosal responses to helminth parasites. Nature 2016 Jan 14;529(7585):226-30. doi: 10.1038/nature16527. PMID: 26762460.
- Gerbe F., van Es J. H., Makrini L., Brulin B., Mellitzer G., Robine S., Romagnolo B., Shroyer N. F., Bourgaux J.-F., Pignodel C., Clevers H. and Jay P. : Distinct ATOH1 and Neurog3 requirements define tuft cells as a new secretory cell type in the intestinal epithelium. J Cell Biol. 2011 Mar 7;192(5):767-80. doi: 10.1083/jcb.201010127. PMID: 21383077. Editorial comment on this article on page 706 of the same issue.
- Escobar M., Nicolas P., Sangar F., Laurent-Chabalier S., Clair P., Joubert D., Jay P. and Legraverend C. : Intestinal epithelial stem cells do not protect a copy of their genome by asymmetric chromosome segregation. Nat Commun. 2011 Mar 29:2:258. doi: 10.1038/ncomms1260. PMID: 21448157.
- Gerbe F., Brulin B., Makrini L., Legraverend C. and Jay P. : DCAMKL-1 expression identifies tuft cells rather than stem cells in the adult mouse intestinal epithelium. Gastroenterology 2009 Dec;137(6):2179-80; author reply 2180-1. doi: 10.1053/j.gastro.2009.06.072. PMID 19879217.



