Les protéines exprimées au niveau de la membrane plasmique sont des transmetteurs essentiels des informations extracellulaires et régulent ainsi la signalisation cellulaire. Leur position à la frontière entre le milieu extracellulaire et intracellulaire en fait aussi des cibles privilégiées lors des premières étapes des interactions hôtes-pathogènes. Ces protéines membranaires jouent ainsi un rôle clé dans la physiologie humaine normale et pathologique.
Dans ce contexte, notre recherche vise à élucider les bases moléculaires de la liaison et de la régulation de l’activité de ces protéines par des approches intégrées de pharmacologie moléculaire et de biologie structurale combinant la biochimie, la RMN, la cristallographie, la cryoEM, la spectrométrie de masse structurale (native et HDX) et la bioinformatique. Nous nous intéressons plus particulièrement à des protéines qui possèdent un fort potentiel pour le développement de molécules à visées thérapeutiques comme les récepteurs couplés aux protéines G (GPCRs) et les enzymes contrôlant l’homéostasie des céramides. Forts de ces connaissances, nous utilisons des approches de chemo-informatique et notamment l’IA, pour identifier des molécules pouvant moduler l’activité et la fonction de ces protéines. Ces molécules constituent à la fois des outils pour étudier la fonction des protéines d’intérêts in vivo et aussi un point de départ pour le développement de molécules à visées thérapeutiques.
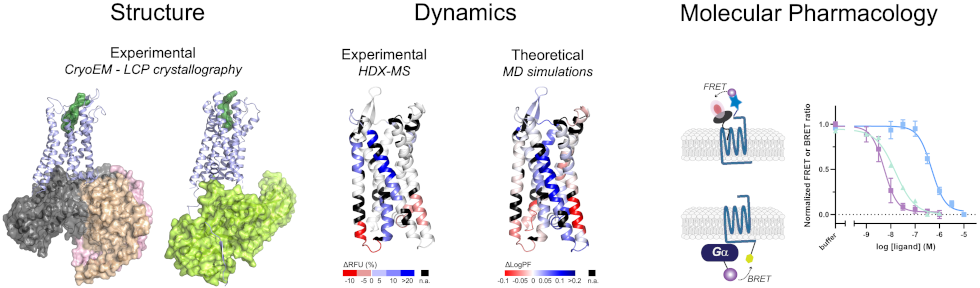
Structure, dynamique et pharmacologie moléculaire de complexes de signalisation de récepteurs couplés aux protéines G (GPCRs) obtenues par cryo-microscopie électronique ou crystallographie en phase cubique lipidique (CryoEM ou LCP), échange Hydrogene/Deuterium couplé à la spectrométrie de masse (HDX-MS), simulations de dynamique moléculaire (MD) et expériences de FRET ou BRET sur cellules vivantes.
Chef d'équipe

DR1, Inserm

IGF Nord 204a

04 34 35 92 80
En savoir plus >

DR2, Inserm

IGF Sud 001

04 34 35 92 68
En savoir plus >
Chercheurs

PU, UM

IGF Sud 025

04 34 35 93 24
En savoir plus >

CRCN, CNRS

IGF Nord 204b

04 34 35 92 80
En savoir plus >

DR2, CNRS

IGF Sud 025

04 34 35 93 45
En savoir plus >

CRCN, Inserm

IGF Nord 226

04 34 35 93 02
En savoir plus >

CRCN, Inserm

IGF Nord 213

04 34 35 92 80
En savoir plus >

CRHC, CNRS

IGF Nord 224

04 34 35 93 20
En savoir plus >

PU-PH2, UM

CHU

04 34 35 92 64
En savoir plus >

CRCN, Inserm

IGF Nord 204b

04 34 35 92 80
En savoir plus >
Techniciens et ingénieurs

IEHC, CNRS

IGF Nord 226a

04 34 35 93 02
En savoir plus >
Chercheurs CDD et doctorants

Doctorant(e), UM

IGF Nord 207c

04 34 35 92 64
En savoir plus >

Chercheur CDD, CNRS

IGF Nord 207c

04 34 35 92 64
En savoir plus >

Chercheur CDD, Inserm

IGF Nord 204a

04 34 35 92 80
En savoir plus >
Techniciens et ingénieurs CDD

IE CDD, Inserm

IGF Nord 204a

04 34 35 92 80
En savoir plus >

IE CDD, Inserm

IGF Nord 207b

04 34 35 92 64
En savoir plus >

IE CDD, Inserm

IGF Nord 207c

04 34 35 92 64
En savoir plus >

IE CDD, CNRS

IGF Nord 209b

04 34 35 92 64
En savoir plus >
Stagiaires

Master 1, UM

IGF Sud 025

04 34 35 93 24
En savoir plus >

Master 1, CNRS

IGF Nord 204a

04 34 35 92 80
En savoir plus >

Stagiaire, CNRS

IGF Nord 226

04 34 35 92 68
En savoir plus >
- Bous J, Fouillen A, Orcel H, Trapani S, Cong X, Fontanel S, Saint-Paul J, Lai-Kee-Him J, Urbach S, Sibille N, Sounier R, Granier S#, Mouillac B#, Bron P#. Structure of the vasopressin hormone-V2 receptor-β-arrestin1 ternary complex. Science Adv. 2022 Sep 2;8(35):eabo7761. doi: 10.1126/sciadv.abo7761. # Co-corresponding authors.
- Healey RD, Saied EM, Cong X, Karsai G, Gabellier L, Saint Paul J, Del Nero E, Jeannot S, Drapeau M, Fontanel S, Maurel D, Basu S, Leyrat C, Golebiowski J, Bossis G, Bechara C, Hornemann T, Arenz C, Granier S. Discovery and mechanism of action of small molecule inhibitors of ceramidases. Angew Chem Int Ed Engl. 2021 Oct 20. doi: 10.1002/anie.202109967.
- Grison CM, Lambey P, Jeannot S, Del Nero E, Fontanel S, Peysson F, Heuninck J, Sounier R, Durroux T, Leyrat C, Granier S#, Bechara C#. Molecular insights into mechanisms of GPCR hijacking by Staphylococcus aureus. Proc Natl Acad Sci U S A. 2021 Oct 19;118(42):e2108856118. doi: 10.1073/pnas.2108856118. # Co-corresponding authors.
- Cong X, Maurel D, Déméné H, Vasiliauskaité-Brooks I, Hagelberger J, Peysson F, Saint-Paul J, Golebiowski J, Granier S#, Sounier R#. Molecular insights into the biased signaling mechanism of the μ-opioid receptor. Mol Cell. 2021 Oct 21;81(20):4165-4175.e6. doi: 10.1016/j.molcel.2021.07.033. Epub 2021 Aug 24. # Co-corresponding authors.
- Bous J, Orcel H, Floquet N, Leyrat C, Lai-Kee-Him J, Gaibelet G, Ancelin A, Saint-Paul J, Trapani S, Louet M, Sounier R, Déméné H, Granier S#, Bron P#, Mouillac B#. Cryo-electron microscopy structure of the antidiuretic hormone arginine-vasopressin V2 receptor signaling complex. Sci Adv. 2021 May 21;7(21). doi: 10.1126/sciadv.abg5628. # Co-corresponding authors.
- Vasiliauskaité-Brooks I, Healey RD, Rochaix P, Saint-Paul J, Sounier R, Grison C, Waltrich-Augusto T, Fortier M, Hoh F, Saied EM, Arenz C, Basu S, Leyrat C, Granier S#. Structure of a human intramembrane ceramidase explains enzymatic dysfunction found in leukodystrophy.Nature Commun. 2018 Dec 21;9(1):5437.
- Vasiliauskaité-Brooks I, Sounier R, Rochaix P, Bellot G, Fortier M, Hoh F, De Colibus L, Bechara C, Saied EM, Arenz C, Leyrat C#, Granier S#. Structural insights into adiponectin receptors suggest ceramidase activity. 2017 Apr 06;544:120-123. doi: 10.1038/nature21714. # Co-corresponding authors.
- Sounier R, Mas C, Steyaert J, Laeremans T, Manglik A, Huang W, Kobilka BK, Déméné H, Granier S. Propagation of conformational changes during μ-opioid receptor activation. Nature. 2015 Aug 20;524(7565):375-8.
- Granier S, Manglik A, Kruse AC, Kobilka TS, Thian FS, Weis WI, Kobilka BK. Structure of the δ-opioid receptor bound to naltrindole. 2012 May 16;485(7398):400-4.
- Manglik A, Kruse AC, Kobilka TS, Thian FS, Mathiesen JM, Sunahara RK, Pardo L, Weis WI, Kobilka BK, Granier S. Crystal structure of the µ-opioid receptor bound to a morphinan antagonist. 2012 Mar 21;485(7398):321-6.

Bases moléculaires et structurales de la fonction des GPCRs
Responsables
Rémy SOUNIER, Thierry DURROUX et Christiane MENDRE
En savoir plus
Récepteurs couplés aux protéines G et pathogènes
Responsable
Chérine BECHARA
En savoir plus
Innovation Thérapeutique
Responsables
Cédric LEYRAT et Xiaojing CONG
En savoir plus




 IGF Nord 204a
IGF Nord 204a 04 34 35 92 80
04 34 35 92 80
 IGF Sud 001
IGF Sud 001 04 34 35 92 68
04 34 35 92 68
 IGF Sud 025
IGF Sud 025 04 34 35 93 24
04 34 35 93 24
 IGF Nord 204b
IGF Nord 204b 04 34 35 92 80
04 34 35 92 80
 IGF Sud 025
IGF Sud 025 04 34 35 93 45
04 34 35 93 45
 IGF Nord 226
IGF Nord 226 04 34 35 93 02
04 34 35 93 02
 IGF Nord 213
IGF Nord 213 04 34 35 92 80
04 34 35 92 80
 IGF Nord 224
IGF Nord 224 04 34 35 93 20
04 34 35 93 20
 CHU
CHU 04 34 35 92 64
04 34 35 92 64
 IGF Nord 204b
IGF Nord 204b 04 34 35 92 80
04 34 35 92 80
 IGF Nord 226a
IGF Nord 226a 04 34 35 93 02
04 34 35 93 02
 IGF Nord 207c
IGF Nord 207c 04 34 35 92 64
04 34 35 92 64
 IGF Nord 207c
IGF Nord 207c 04 34 35 92 64
04 34 35 92 64
 IGF Nord 204a
IGF Nord 204a 04 34 35 92 80
04 34 35 92 80
 IGF Nord 204a
IGF Nord 204a 04 34 35 92 80
04 34 35 92 80
 IGF Nord 207b
IGF Nord 207b 04 34 35 92 64
04 34 35 92 64
 IGF Nord 207c
IGF Nord 207c 04 34 35 92 64
04 34 35 92 64
 IGF Nord 209b
IGF Nord 209b 04 34 35 92 64
04 34 35 92 64
 IGF Sud 025
IGF Sud 025 04 34 35 93 24
04 34 35 93 24
 IGF Nord 204a
IGF Nord 204a 04 34 35 92 80
04 34 35 92 80
 IGF Nord 226
IGF Nord 226 04 34 35 92 68
04 34 35 92 68