La douleur chronique, dont la prévalence est de 20 à 30 %, est la principale cause de souffrance humaine dans le monde. Les traitements actuels demeurent limités pour ces douleurs pathologiques. Pour mieux comprendre les voies neuronales de la douleur et leur dysfonctionnement pathologiques, notre équipe explore l’impact de canaux ioniques régulant l’entrée de calcium dans les cellules. Ces canaux sont des protéines essentielles pour l’initiation, la propagation et la transmission des informations de neurones en neurones. Nous visons à comprendre l’impact des canaux calciques dans la pathophysiologie de la douleur en se concentrant sur les neurones sensoriels périphériques et sur les circuits spinaux en utilisant la génétique de la souris, l’électrophysiologie, la pharmacologie la biochimie, et le comportement dans des modèles précliniques de douleur chronique. De plus la présence du canal Cav3.2 au centre de nos projets dans des sous types de neurones sensoriels dévolus à la perception des stimuli mécaniques intègre nos travaux dans l’élucidation des mécanismes moléculaires du sens du toucher au-delà de la thématique douleur. Nous sommes convaincus que les résultats précliniques doivent être validés dans des tissus humains pour renforcer leur crédibilité dans des perspectives cliniques. Ainsi, nous développons en lien avec l’hôpital de Montpellier des explorations moléculaires et fonctionnelles ex vivo dans les neurones sensoriels et la moelle épinière humaine prélevés sur des donneurs d’organes. En parallèle, nous étudions des atteintes auto-immunes des neurones du système nerveux périphérique pour comprendre le mécanisme d’action des auto anticorps des patients. Ainsi, nous positionnons donc notre recherche sur une stratégie translationnelle priorisant les voies moléculaires conservées entre les modèles animaux et les humains afin de maximiser nos chances de découvrir les mécanismes de la physiopathologie de la douleur.
Axe 1
Les questions abordées autour de rôle des canaux calciques à bas seuil d’activation concernent :
1) leur impact dans les neurones sensoriels mécanorécepteurs cutanés et viscéraux
2) leurs rôles dans les réseaux neuronaux spinaux pour l’intégration de l’information sensorielle
3) leur participation à l’excitabilité des circuits supraspinaux activés par les mécanorécepteurs
Ces questions sont abordées en utilisant de modèles précliniques douleurs proches de la clinique et en utilisant des tissus humains pour valider les travaux précliniques.
Axe 2
En parallèle, nous étudions les atteintes d’origine auto-immunes des neurones périphériques en se focalisant sur les nodopathies démyélinisantes. Cette approche est directement intégrée à la clinique en caractérisant des sérums de patients souffrant de ces pathologies douloureuses.
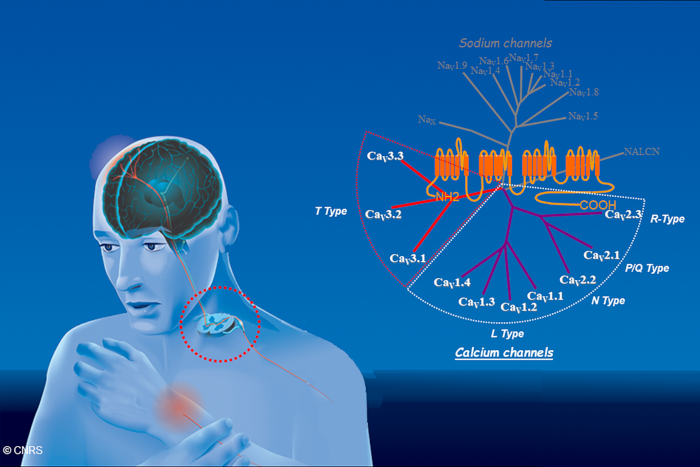
Diversité moléculaire des sous-unités canalaires des canaux calciques (CaV) appartenant à la super famille des canaux à 4 domaines transmembranaires. Notre activité de recherche vise à identifier le rôle de ces canaux dans les neurones sensoriels afférents primaires, et les neurones de la moelle épinières premiers maillons dans la perception de la douleur.
Chef d'équipe

DR1, CNRS

IGF Sud 125

04 34 35 92 48
En savoir plus >
Chercheurs

CRCN, CNRS

IGF Sud 125

04 34 35 92 48
En savoir plus >

DR2, CNRS

IGF Sud 125

04 34 35 92 48
En savoir plus >

Collaborateur, Inserm

IGF Sud 125

04 34 35 92 48
En savoir plus >

PU-PH1, UM

IGF Sud 125

04 34 35 92 48
En savoir plus >

CRCN, Inserm

IGF Sud 125

04 34 35 92 48
En savoir plus >

Collaborateur, CHU

IGF Sud 125

04 34 35 92 48
En savoir plus >
Chercheurs CDD et doctorants

Doctorant(e), Inserm

IGF Sud 125

04 34 35 92 48
En savoir plus >

Gawain
Grellier Cavaignac
Doctorant(e), Inserm

IGF Sud 125

04 34 35 92 48
En savoir plus >

Doctorant(e), CHU

IGF Sud 125

04 34 35 92 48
En savoir plus >

Doctorant(e), Inserm

IGF Sud 125

04 34 35 92 48
En savoir plus >
Techniciens et ingénieurs CDD

IE CDD, Inserm

IGF Sud 125

04 34 35 92 48
En savoir plus >
Stagiaires

Stagiaire, Inserm

IGF Sud 125

04 34 35 92 48
En savoir plus >
- Yadav, K. J. E. Matson, L. Li, I. Hua, J. Petrescu, K. Kang, M. R. Alkaslasi, D. I. Lee, S. Hasan, A. Galuta, A. Dedek, S. Ameri, J. Parnell, M. M. Alshardan, F. A. Qumqumji, S. M. Alhamad, A. P. Wang, G. Poulen, N. Lonjon, F. Vachiery-Lahaye, P. Gaur, M. A. Nalls, Y. A. Qi, D. Maric, M. E. Ward, M. E. Hildebrand, P. F. Mery, E. Bourinet, L. Bauchet, E. C. Tsai, H. Phatnani, C. E. Le Pichon, V. Menon and A. J. Levine. A cellular taxonomy of the adult human spinal cord. Neuron 2023 111, 328-344 e7. 10.1016/j.neuron.2023.01.007, PMC10044516.
- Huzard, M. Martin, F. Maingret, J. Chemin, F. Jeanneteau, P. F. Mery, P. Fossat, E. Bourinet and A. Francois. The impact of C-tactile low-threshold mechanoreceptors on affective touch and social interactions in mice. Sci Adv 2022 8, eabo7566. 10.1126/sciadv.abo7566, PMC9242590.
- L. Fayad, G. Ourties, B. Le Gac, B. Jouffre, S. Lamoine, A. Fruquiere, S. Laffray, L. Gasmi, B. Cauli, C. Mallet, E. Bourinet, T. Bessaih, R. C. Lambert and N. Leresche. Centrally expressed Cav3.2 T-type calcium channel is critical for the initiation and maintenance of neuropathic pain. Elife 2022 11. 10.7554/eLife.79018, PMC9714965.
- Defaye, M. C. Iftinca, V. M. Gadotti, L. Basso, N. S. Abdullah, M. Cumenal, F. Agosti, A. Hassan, R. Flynn, J. Martin, V. Soubeyre, G. Poulen, N. Lonjon, F. Vachiery-Lahaye, L. Bauchet, P. F. Mery, E. Bourinet, G. W. Zamponi and C. Altier. The neuronal tyrosine kinase receptor ligand ALKAL2 mediates persistent pain. J Clin Invest 2022 132. 10.1172/JCI154317, PMC9197515.
- Beaulieu-Laroche, M. Christin, A. Donoghue, F. Agosti, N. Yousefpour, H. Petitjean, A. Davidova, C. Stanton, U. Khan, C. Dietz, E. Faure, T. Fatima, A. MacPherson, S. Mouchbahani-Constance, D. G. Bisson, L. Haglund, J. A. Ouellet, L. S. Stone, J. Samson, M. J. Smith, K. Ask, A. Ribeiro-da-Silva, R. Blunck, K. Poole, E. Bourinet and R. Sharif-Naeini. TACAN Is an Ion Channel Involved in Sensing Mechanical Pain. Cell 2020 180, 956-967 e17. 10.1016/j.cell.2020.01.033.
- Candelas, A. Reynders, M. Arango-Lievano, C. Neumayer, A. Fruquiere, E. Demes, J. Hamid, C. Lemmers, C. Bernat, A. Monteil, V. Compan, S. Laffray, P. Inquimbert, Y. Le Feuvre, G. W. Zamponi, A. Moqrich, E. Bourinet and P. F. Mery. Cav3.2 T-type calcium channels shape electrical firing in mouse Lamina II neurons. Sci Rep 2019 9, 3112. 10.1038/s41598-019-39703-3, PMC6395820.
- Francois, N. Schuetter, S. Laffray, J. Sanguesa, A. Pizzoccaro, S. Dubel, A. Mantilleri, J. Nargeot, J. Noel, J. N. Wood, A. Moqrich, O. Pongs and E. Bourinet. The Low-Threshold Calcium Channel Cav3.2 Determines Low-Threshold Mechanoreceptor Function. Cell Rep 2015 10, 370-382. 10.1016/j.celrep.2014.12.042.
- Garcia-Caballero, V. M. Gadotti, P. Stemkowski, N. Weiss, I. A. Souza, V. Hodgkinson, C. Bladen, L. Chen, J. Hamid, A. Pizzoccaro, M. Deage, A. Francois, E. Bourinet and G. W. Zamponi. The deubiquitinating enzyme USP5 modulates neuropathic and inflammatory pain by enhancing Cav3.2 channel activity. Neuron 2014 83, 1144-58. 10.1016/j.neuron.2014.07.036.
- Descoeur, V. Pereira, A. Pizzoccaro, A. Francois, B. Ling, V. Maffre, B. Couette, J. Busserolles, C. Courteix, J. Noel, M. Lazdunski, A. Eschalier, N. Authier and E. Bourinet. Oxaliplatin-induced cold hypersensitivity is due to remodelling of ion channel expression in nociceptors. EMBO Mol Med 2011 3, 266-78. 10.1002/emmm.201100134, PMC3377073.
- Bourinet, A. Alloui, A. Monteil, C. Barrere, B. Couette, O. Poirot, A. Pages, J. McRory, T. P. Snutch, A. Eschalier and J. Nargeot. Silencing of the Cav3.2 T-type calcium channel gene in sensory neurons demonstrates its major role in nociception. EMBO J 2005 24, 315-24. 10.1038/sj.emboj.7600515, PMC545807.




 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48
 IGF Sud 125
IGF Sud 125 04 34 35 92 48
04 34 35 92 48


