Équipe Stéphanie BARRÈRE-LEMAIRE – Matteo MANGONI
Cardioprotection, physiopathologie du rythme cardiaque et ischémie
Projet Comprendre la physiopathologie du mécanisme à la base de l’automatisme cardiaque pour une meilleure prise en charge de la dysfonction sino-auriculaire et les blocs auriculo-ventriculaires
RESPONSABLE

Personnel IGF impliqué
Matteo MANGONI
DR1 CNRS
Joël NARGEOT
DRCE CNRS
Isabelle BIDAUD
IECE Inserm
Eleonora TORRE
Postdoc CNRS
Giuseppe ANGELINI
Postdoc CNRS
Pinidmontree CHIRUTCHAYA
Doctorante (Univ. Chulalongkorn, Thaïlande)
Nadia MEKRANE
Doctorante UM
Leila TALSSI
IE CDD Inserm
Eliane MORAIS-PINTO
Doctorante UM
Mon projet de recherche a trois buts principaux : a) Caractériser le rôle des différents canaux ioniques et des protéines liées à la dynamique calcique intracellulaire dans l’activité pacemaker cardiaque ; b) Améliorer les approches pharmacologiques et génétiques pour corriger la bradycardie dans nos modèles de dysfonction du nœud sino-atrial et du nœud atrio-ventriculaire c) Explorer une nouvelle voie de recherche basée sur les cardiomyocytes automatiques d’origine humaine (hIPSC) afin de développer de nouvelles thérapies contre la bradycardie en ciblant les canaux IKACh (GIRK4). Mes résultats permettront : 1) d’améliorer la compréhension des aspects encore inconnus du mécanisme pacemaker et 2) d’ouvrir de nouvelles perspectives dans la recherche clinique pour le traitement des dysfonctions du nœud sino-atrial et de la conduction du signal.
Caractérisation du rôle fonctionnel des différents canaux ioniques et des protéines liées à la dynamique calcique intracellulaire dans la génération/régulation de l’automatisme cardiaque
L’objectif de ce projet de recherche est de clarifier le rôle de l’association fonctionnelle entre différents canaux ioniques impliqués dans la génération de l’automatisme cardiaque et sa régulation par le système nerveux autonome. Grâce à des approches électrophysiologiques (in vitro, ex vivo et in vivo) et moléculaires, nous étudions l’effet de différentes toxines peptidiques dérivées de venins animaux sur la régulation de la fréquence cardiaque. Le ciblage des canaux ioniques voltage-dépendants du le nœud sino-atrial par ces toxines ouvre de nouvelles perspectives pour le contrôle spatiotemporel du rythme cardiaque.
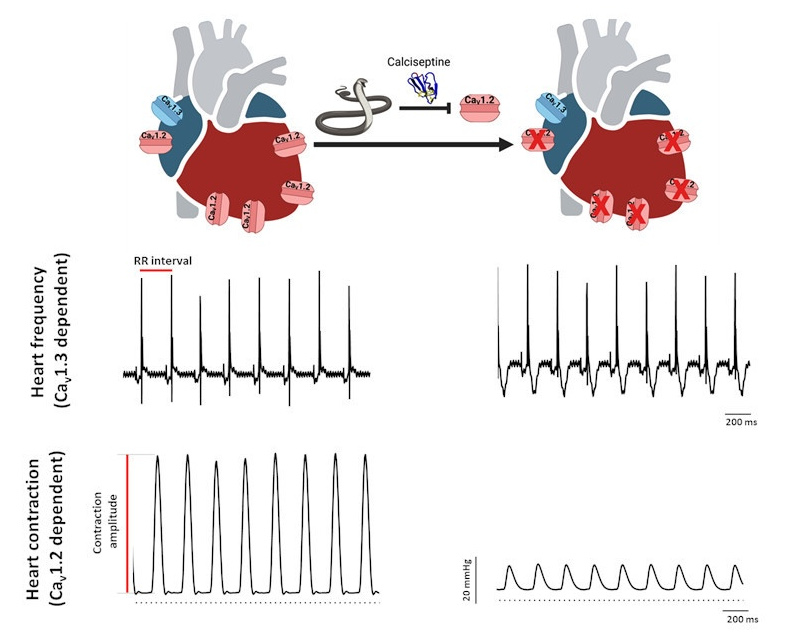
Enregistrement de la fréquence cardiaque (ECG) et de la contraction d’un cœur perfusé avec de la Calciseptine, une toxine dérivée du venin de mamba noir. Tracés représentatifs de l’ECG (en haut) et de l’enregistrements de pression (en bas) d’un cœur perfusé isolé en condition ctrl (gauche) et en présence de Calciseptine (droite).
Principales publications
• Mesirca P., et al. (2024), Nat Commun, 15(1), 54.
• Montnach J. et al. (2023), Circ Res, 133(6), 535
Financements
• 2024-2025 Royal Golden Jubilee (RGJ) Ph.D. scholarship from the National Research Council of Thailand under the Ministry of Higher Education, Science, Research and Innovation
• 2020-2025 TNE FANTASY-Fondation Leducq
• 2015-2024 ANR- LABEX-ICST
Collaborations
• Kittipong Tachampa (Bangkok, Thailand)
• Jerome Montnach (Nantes, France)
Alumni
• Eliane MORAIS-PINTO (M2, 2024)
• Chirutchaya PINIDMONTREE (PhD student, 2024-2025)
• Julien LOURADOUR (PhD, 2016-2020)
• Matthias BAUDOT (PhD, 2015-2019)
Correction de la bradycardie (par voie pharmacologique) pour rétablir la fonction sinusale dans des modèles de dysfonction du nœud sino-atrial et du nœud atrio-ventriculaire
Ce projet de recherche est dédié à l’étude de nouvelles stratégies pour corriger la dysfonction sinusale (SND) par inhibition du courant IKACh (GIRK4) La SND est causée par l’échec du NSA à générer un potentiel d’action normal. A ce jour, la seule thérapie disponible pour traiter la SND chronique consiste en l’implantation d’un stimulateur cardiaque.
Nous testons de nouveaux modulateurs d’IKACh dans des modèles de bradycardie et d’arythmies causées par des dysfonctions du NSA et du NAV. Ces modèles sont déjà disponibles dans notre équipe. Le but ultime du projet est de développer de nouveaux agents pharmacologiques ciblant les canaux GIRK4 pour proposer une thérapie innovante dans la prise en charge de la bradycardie induite par la SND et les arythmies associées chez les patients.
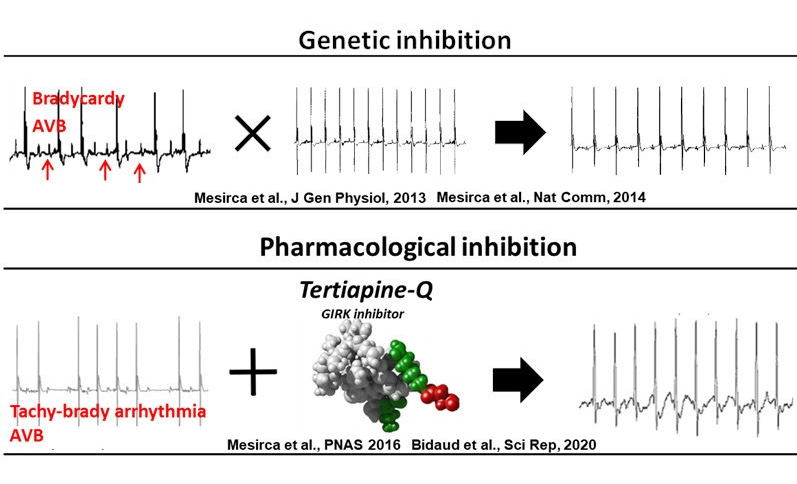
Ciblage génétique et pharmacologique des canaux GIRK4 dans deux modèles différents de bradycardie et dysfonctionnement sinusale : HCN4-AYA and Cav1.3-/-. L’inhibition du canal GIRK4 corrige la bradycardie et les défauts de conduction cardiaque dans ces deux modèles.
Principales publications
• Bidaud I., et al. (2021) Front Physiol, 11, 519382.
• Bidaud I., et al. (2020) Sci Rep, 10(1), 9835.
• Mesirca P., et al. (2016) Proc Natl Acad Sci USA, 113(7), E932.
• Mesirca P., et al. (2014) Nat Commun, 5, 4664
Financements
• 2020-2025 TNE FANTASY-Fondation Leducq
• 2015-2024 ANR- LABEX-ICST
Collaborations
• Alicia D’SOUZA (London, UK)
• Michel DE WAARD (Nantes, France)
• Nelly PIROT (Montpellier, France)
Alumni
• Olivier BORTOLOTTI (M1, 2021)
• Eleonora TORRE (PhD, 2019)
• Leila TALSSI (PhD, 2018-2021)
• Antony CHUNG YOU CHONG (PhD, 2015-2019)
Caractérisation des cardiomyocytes pacemaker-like patient-spécifique iPSC-dérivés pour le traitement de la dysfonction sinusale
En se basant sur nos découvertes précédentes montrant que l’ablation génétique et l’inhibition pharmacologique des canaux IKACh (GIRK4) normalise la fréquence cardiaque et prévient la bradyarrythmie dans des modèles des dysfonction sinusale (SND), nous souhaitons explorer une nouvelle voie de recherche basée sur les cardiomyocytes automatiques d’origine humaine (hIPSC) afin de proposer de nouvelles thérapies pour corriger la bradycardie en ciblant les canaux GIRK4. Pour ce faire, nous développons un modèle in vitro de SND primaire en utilisant des cardiomyocytes automatiques d’origine humaine dérivés du patient pour mettre au point une nouvelle thérapie personnalisée, basée sur les gènes, pour normaliser l’automaticité cardiaque.
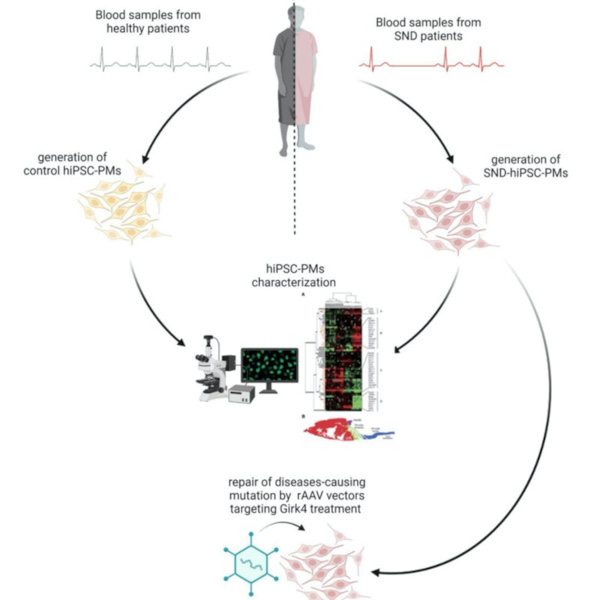
Schéma résumant les objectifs du projet : 1. Amélioration du protocole pour orienter la différenciation des cardiomyocytes (hIPSC) vers une population enrichie en cardiomyocytes pacemaker-like (hiPSC-PMs). 2. Génération de modèles humains de SND in vitro basés sur des hiPSC-PMs dérivés de patients ayant des antécédents de SND primaire et portant différentes mutations dans les canaux ioniques impliquée dans le pacemaking. 3. Développement d’une thérapie génique à long terme basée sur de vecteurs pour l’ablation génétique de l’IKACh afin de corriger la SND.
Principales publications
• Torre E., et al. (2024) Int J Mol Sci, 25(6), 3387.
Financements
• 2022-2025 ANR FENICE
Collaborations
• Albano MELI (Montpellier, Fance)
• Nathalie NEYROUD (Paris, France)
• Romain DESPRAT (Montpellier, France)
Alumni
• Nadia MEKRANE (PhD, 2023-2026)


