Dans le cadre de l’appel d’offre « IMPACT SANTE » de l’Inserm, un programme de financement de la recherche de rupture, à risque et à impact en santé, Cédric Leyrat, chercheur dans l’équipe animée par Sébastien Granier et Bernard Mouillac, participe au projet AIR-MT. Ce projet, financé à hauteur de 3 Millions d’Euros, est coordonné par Bruno Canard (AFMB, Marseille), en collaboration avec Renaud Vincentelli (AFMB, Marseille), Olivier Schwartz (Institut Pasteur, Paris), Béatrice Nal (CIML, Marseille) et Cédric Leyrat (IGF, Montpellier).
Les ARN messagers (ARNm) sont des molécules intrinsèquement instables dont la fonction et la stabilité sont régulées par plus de 100 modifications post-transcriptionnelles connues, y compris les méthylations de l’ARN. Ces dernières années, les thérapies et les vaccins à base d’ARNm ont révolutionné la médecine, soulignant la nécessité d’un contrôle précis de la stabilité des ARNm synthétiques et d’une fonctionnalisation sélective pour garantir une efficacité cellulaire optimale. Le projet AIR-MT vise à relever ce défi en exploitant la méthylation de l’ARN site-spécifique pour améliorer à la fois la stabilité de l’ARNm et l’équilibre entre l’activation de la réponse immunitaire et l’expression des protéines du non-soi.
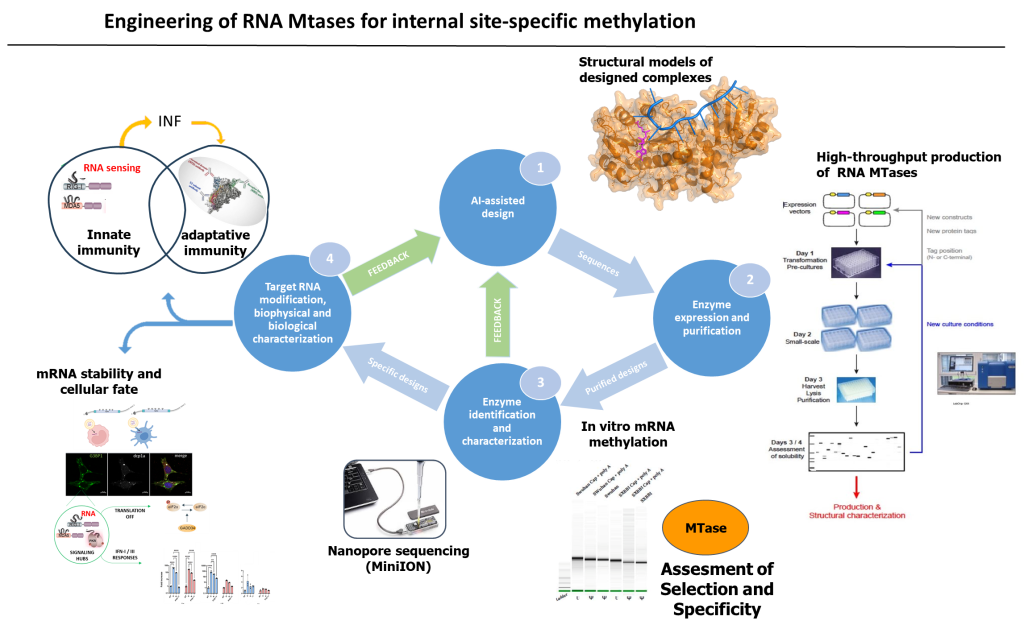
Mise en oeuvre du projet AIR-MT. La conception assistée par l’IA génère des échafaudages virtuels (1). Les gènes synthétiques sont commandés, exprimés et les RMTases putatives sont produites, purifiées (2) et leur spécificité est analysée à l’aide de divers substrats d’ARN. Les ARNm vaccinaux synthétiques sont modifiés et la spécificité site/atome des RMTases est déterminée (3). Ces ARNm modifiés sont ensuite évalués et l’induction de la réponse antivirale, impliquant l’immunité innée et le système immunitaire, est disséquée (4). Ceci constitue une boucle dans le processus itératif, où les RMTases prometteuses sont utilisées pour modifier les ARNm avec des propriétés biophysiques et biologiques améliorées. Les cycles de caractérisation effectués en (3) et (4) fournissent un retour d’information à l’étape (1) (flèches vertes).
Le concept clé d’AIR-MT est de développer des méthyltransférases d’ARN site-spécifiques (RMTases) capables de modifier les ARNm pour qu’ils résistent à la dégradation chimique et à la dégradation par nucléase tout en conférant des propriétés immunologiques souhaitables pour les futurs traitements et vaccins à base d’ARNm. Le projet exploitera les récentes percées dans le domaine de la conception d’enzymes guidée par l’intelligence artificielle pour créer des RMTases synthétiques ayant des activités spécifiques ciblant des modifications clés de l’ARN, notamment la m6A (N6-méthyladénosine), la m1A (N1-méthyladénosine), la m5C (5-méthylcytidine), et la Nm (2′-O-méthylation). Ces enzymes modifiées seront criblées et optimisées à l’aide de méthodes à haut débit.
Pour démontrer la faisabilité et l’impact de cette approche, AIR-MT se concentrera sur une cible ARN bien définie et cliniquement pertinente : l’ARNm Spike du SRAS-CoV-2, qui a joué un rôle déterminant dans les efforts de vaccination à l’échelle mondiale. En identifiant les régions fragiles et immunogènes dans la séquence de l’ARN et en les méthylant de manière sélective, le projet vise à générer de nouvelles molécules d’ARNm présentant une stabilité accrue, une évasion immunitaire optimisée et une efficacité de traduction améliorée. Ces ARNm modifiés seront évalués dans des modèles cellulaires et animaux, ouvrant la voie à des vaccins de nouvelle génération, à des ARN thérapeutiques et à des outils innovants pour la recherche biomédicale.
Au-delà de l’acquisition de connaissances fondamentales sur la modification des ARN et la stabilité des ARNm, AIR-MT devrait contribuer au développement de thérapies à base d’ARNm plus efficaces et plus durables, avec de vastes applications dans le développement de vaccins et le traitement de diverses maladies.


