Les effets secondaires des médicaments sont souvent dus à des interactions involontaires avec de mauvaises cibles dans notre organisme. Les médicaments modernes sont de plus en plus spécifiques à leurs cibles, grâce aux efforts considérables de la recherche pour réduire les effets secondaires. Toutefois, l’action des médicaments même sur leur cible, peut encore produire des effets secondaires, parfois graves. Ces dernières années par exemple, les analgésiques opioïdes ont causé plus de 70 000 décès aux États-Unis en 2019.
En Europe, une « épidémie silencieuse d’opioïdes » suscite également des inquiétudes. En effet, les opioïdes agissent sur nos récepteurs opioïdes, qui contrôlent non seulement la douleur, mais aussi la récompense, la dépendance, l’humeur et encore d’autres fonctions. Comme la plupart des cibles médicamenteuses (sinon toutes), les récepteurs opioïdes sont des dispositifs moléculaires multifonctionnels de taille nanométrique. Où se trouve donc le bouton spécifique anti-douleur sans effets secondaires ?
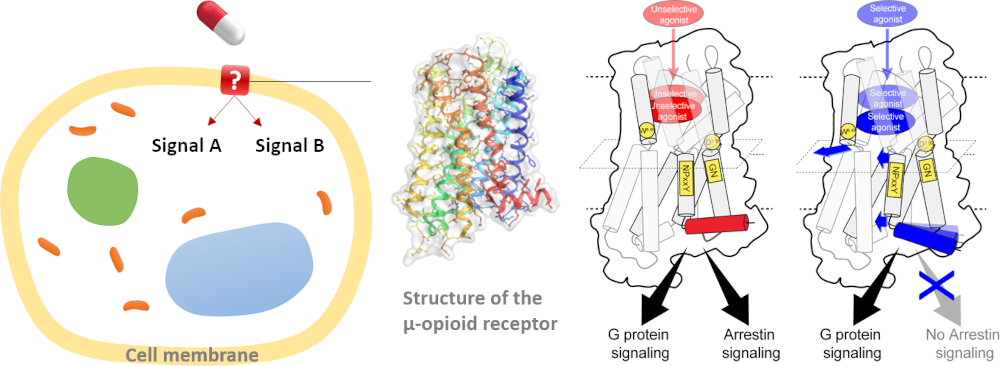
L’équipe du Dr Sébastien Granier au sein de l’Institut de génomique fonctionnelle vient de faire un grand pas vers cette réponse. Les récepteurs opioïdes sont des récepteurs couplés aux protéines G (RCPG). Les RCPG sont des protéines à la surface des cellules qui régulent les réponses cellulaires aux stimuli extracellulaires. Les humains possèdent 800 types de RCPG, qui contiennent les cibles de ~40% des médicaments commercialisés. Cette famille de protéines partage une architecture tridimensionnelle et deux principales voies de signalisation à l’intérieur des cellules. Sous l’effet de stimuli (par exemple, des molécules médicamenteuses), un RCPG peut adopter différentes conformations, qui ouvrent/ferment les voies de signalisation de manière spécifique pour déclencher différentes réponses cellulaires et réactions corporelles. La nature nous a donné des dispositifs aussi délicats, mais sans les manuels.
En 2012, le Dr Granier et ses collègues ont obtenu les premières structures 3D à haute résolution des récepteurs opioïdes. En 2015, son équipe a mis au point une stratégie permettant d’observer les changements de conformation du récepteur µ-opioïde pendant sa réponse aux analgésiques opioïdes. Cette année, l’équipe vient de découvrir comment différents analgésiques ouvrent/ferment séparément les deux principales voies du récepteur (et déclenchent des réponses cellulaires différentes), en agissant sur un point idéal au cœur du récepteur.
Ce travail, publié dans la revue Molecular Cell, combine des simulations informatiques (~2 mois de calculs sur l’un des supercalculateurs les plus rapides de France, OCCIGEN), la spectroscopie RMN et des essais de pharmacologie sur cellules vivantes. Elle décrit le mécanisme de ce nanodispositif dans les moindres détails.
Pour voir une présentation 3D, cliquez ici. L’équipe cherche maintenant à savoir si ce mécanisme est universel pour d’autres RCPG. La compréhension de plus en plus précise de ces cibles permettra de futurs médicaments de plus en plus spécifiques.
Lien publication : Molecular insights into the biased signalling mechanism of the m-opioid receptor (Molecular Cell, septembre 2021)
On en parle dans la presse :
- Communiqué de Presse Inserm : 7/09/2021
- LE FIGARO santé : 20/09/2021
- Vidéo « Biased signaling mechanism of the mu-opioid receptor » sur ce lien
- Pour la Science sur ce lien
- EURACTIV sur ce lien
- UNIVADIS sur ce lien
- [Podcast] A LUM LA SCIENCE #2 : Des opioïdes sans effets secondaires à la plateforme d’expérimentation en économie


